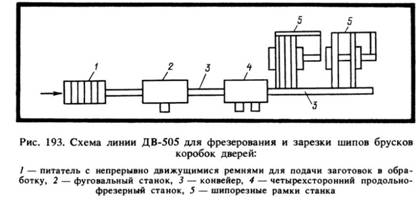
தள பிரிவுகள்
ஆசிரியர்களின் தேர்வு:
- அபார்ட்மெண்ட் வளைகுடாவிற்கான சேதத்தின் அளவை நிர்வாக நிறுவனத்திடமிருந்து மீட்டெடுப்பதற்கான நீதிமன்ற முடிவு
- ஒரு அறையில் வாழ்க்கை அறை மற்றும் குழந்தைகள் அறை: பகிர்வுகளுக்கான விருப்பங்கள்
- சிறந்த மெத்தை சோஃபாக்களின் மதிப்பீடு: வாடிக்கையாளர் மதிப்புரைகள்
- கட்டிடங்களில் விரிவாக்க மூட்டுகள்
- ஷேபர் - அது என்ன, அதன் நோக்கம்
- மர ஆலைகளை கூர்மைப்படுத்துதல்: அரைக்கும் சக்கரங்கள் மற்றும் அரைக்கும் இயந்திரத்தைப் பயன்படுத்தி கையேடு வேலை
- பெல்ட்கள் மற்றும் சாண்ட்ரிக்ஸ், பட்டாசுகள் மற்றும் தொகுதிகள் - கட்டிடக்கலையில் பழைய சரடோவ் சாண்ட்ரிகியின் எடுத்துக்காட்டில் கட்டிடக்கலை ரகசிய குறியீடுகள்
- மேற்பரப்பு அளவிடுதல் - உலோக வேலை
- ஒரு பால்கனி ஸ்லாப்பில் அதிகபட்ச சுமை: ஒரு பேனல் வீட்டில் ஒரு பால்கனியை எவ்வளவு தாங்க முடியும்?
- திட்டங்கள்: நீர் வழங்கல் மற்றும் கழிவுநீருக்கான வரைபடங்கள் பற்றிய புராணக்கதை
விளம்பரம்
| எதிர்ப்பு எவ்வாறு வெப்பநிலையைப் பொறுத்தது. வெப்பநிலையில் உலோகங்களின் எதிர்ப்பின் சார்பு. எதிர்ப்பு ஏன் அதிகரிக்கிறது என்பதைப் புரிந்து கொள்ள முயற்சிப்போம் |
|
கடத்தியின் வெப்பநிலை அதிகரிக்கும் போது, அணுக்களுடன் இலவச எலக்ட்ரான்களின் மோதல்களின் எண்ணிக்கை அதிகரிக்கிறது. எனவே, சராசரி திசை எலக்ட்ரான் வேகம் குறைகிறது, இது கடத்தியின் எதிர்ப்பின் அதிகரிப்புக்கு ஒத்திருக்கிறது. மறுபுறம், அதிகரிக்கும் வெப்பநிலையுடன், கடத்தியின் ஒரு யூனிட் தொகுதிக்கு இலவச எலக்ட்ரான்கள் மற்றும் அயனிகளின் எண்ணிக்கை அதிகரிக்கிறது, இது கடத்தியின் எதிர்ப்பில் குறைவுக்கு வழிவகுக்கிறது. அதிகரிக்கும் வெப்பநிலையுடன், ஒரு காரணி அல்லது இன்னொரு காரணியைப் பொறுத்து, எதிர்ப்பு அதிகரிக்கிறது (உலோகங்கள்), அல்லது குறைகிறது (நிலக்கரி, எலக்ட்ரோலைட்டுகள்), அல்லது கிட்டத்தட்ட மாறாமல் உள்ளது (உலோக உலோகக் கலவைகள், எடுத்துக்காட்டாக மங்கைன்). வெப்பநிலையில் சிறிய மாற்றங்களுடன் (0-100 ° C), 1 ° C வெப்பமாக்குதலுடன் தொடர்புடைய எதிர்ப்பின் அதிகரிப்பு, எதிர்ப்பின் வெப்பநிலை குணகம் என அழைக்கப்படுகிறது, இது பெரும்பாலான உலோகங்களுக்கு மாறாமல் இருக்கும். குறிக்கிறது - வெப்பநிலையில் எதிர்ப்பு, அதிகரிக்கும் வெப்பநிலையுடன் எதிர்ப்பின் ஒப்பீட்டு அதிகரிப்பின் வெளிப்பாட்டை நாம் எழுதலாம்:
பல்வேறு பொருட்களுக்கான எதிர்ப்பின் வெப்பநிலை குணகத்தின் மதிப்புகள் அட்டவணையில் கொடுக்கப்பட்டுள்ளன. 2-2. (2-18) வெளிப்பாட்டிலிருந்து அது பின்வருமாறு
இதன் விளைவாக வரும் சூத்திரம் (2-20) அதன் எதிர்ப்பை கொடுக்கப்பட்ட அல்லது அறியப்பட்ட மதிப்புகளில் அளவிடப்பட்டால் கம்பியின் வெப்பநிலையை (முறுக்கு) தீர்மானிக்க உதவுகிறது. எடுத்துக்காட்டு 2-3. கோட்டின் நீளம் 400 மீ, மற்றும் செப்பு கம்பிகளின் குறுக்குவெட்டு என்றால் வெப்பநிலையில் காற்று-குச்சி கம்பிகளின் எதிர்ப்பை தீர்மானிக்கவும் வெப்பநிலையில் வரி கம்பிகளின் எதிர்ப்பு எதிர்ப்பு சக்தி, எனவே உலோகங்களின் எதிர்ப்பு, வெப்பநிலையைப் பொறுத்தது, அதன் வளர்ச்சியுடன் அதிகரிக்கிறது. கடத்தியின் எதிர்ப்பின் வெப்பநிலை சார்பு என்பது உண்மையால் விளக்கப்படுகிறது
அனுபவம் மிக அதிகமாக இல்லை மற்றும் மிகக் குறைந்த வெப்பநிலையில் இல்லை, வெப்பநிலையின் எதிர்ப்பின்மை மற்றும் கடத்தி எதிர்ப்பின் சார்புகள் சூத்திரங்களால் வெளிப்படுத்தப்படுகின்றன: \\ (~ ho rho_t = \\ rho_0 (1 + \\ ஆல்பா டி), \\) \\ (~ R_t = R_0 (1 + \\ ஆல்பா டி), \\) எங்கே ρ 0 , ρ t என்பது கடத்தி பொருளின் எதிர்ப்புகள் முறையே 0 ° C மற்றும் டி ° C; ஆர் 0 , ஆர் t என்பது 0 ° C மற்றும் கடத்தியின் எதிர்ப்பாகும் டி . சி α - எதிர்ப்பின் வெப்பநிலை குணகம்: முதல் பட்டம் (கே -1) கழிப்பதற்காக கெல்வினில் எஸ்.ஐ.யில் அளவிடப்படுகிறது. உலோகக் கடத்திகளுக்கு, இந்த சூத்திரங்கள் 140 K மற்றும் அதற்கு மேற்பட்ட வெப்பநிலையிலிருந்து தொடங்கி பொருந்தும். வெப்பநிலை குணகம் ஒரு பொருளின் எதிர்ப்பானது, பொருளின் வகையை வெப்பமாக்குவதன் மூலம் எதிர்ப்பின் மாற்றத்தின் சார்புநிலையை வகைப்படுத்துகிறது. இது 1 K ஆல் வெப்பப்படுத்தப்படும்போது கடத்தியின் எதிர்ப்பின் (எதிர்ப்பின்) ஒப்பீட்டு மாற்றத்திற்கு எண்ணியல் ரீதியாக சமமாகும். \\ (~ th mathcal h \\ alpha \\ mathcal i = \\ frac (1 \\ cdot \\ Delta \\ rho) (\\ rho \\ Delta T), \\) இங்கு \\ (~ th mathcal h \\ alpha \\ mathcal i \\) என்பது இடைவெளியில் எதிர்ப்பின் வெப்பநிலை குணகத்தின் சராசரி மதிப்பு Τ . அனைத்து உலோக கடத்திகளுக்கும் α \u003e 0 மற்றும் வெப்பநிலையுடன் சிறிது மாறுகிறது. தூய உலோகங்கள் α = 1/273 கே -1. உலோகங்களில், இலவச கட்டண கேரியர்களின் செறிவு (எலக்ட்ரான்கள்) n = const மற்றும் அதிகரிப்பு ρ படிக லட்டியின் அயனிகளில் இலவச எலக்ட்ரான்களின் சிதறல் தீவிரத்தின் அதிகரிப்பு காரணமாக ஏற்படுகிறது. எலக்ட்ரோலைட் தீர்வுகளுக்கு α < 0, например, для 10%-ного раствора поваренной соли α = -0.02 கே -1. எலக்ட்ரோலைட்டுகளின் எதிர்ப்பு அதிகரிக்கும் வெப்பநிலையுடன் குறைகிறது, ஏனெனில் மூலக்கூறுகளின் விலகல் காரணமாக இலவச அயனிகளின் எண்ணிக்கையில் அதிகரிப்பு கரைப்பான் மூலக்கூறுகளுடன் மோதல்களில் அயனி சிதறலின் வளர்ச்சியை மீறுகிறது. சார்பு சூத்திரங்கள் ρ மற்றும் ஆர் எலக்ட்ரோலைட்டுகளுக்கான வெப்பநிலை உலோகக் கடத்திகளுக்கான மேற்கண்ட சூத்திரங்களைப் போன்றது. இந்த நேரியல் சார்பு ஒரு சிறிய வெப்பநிலை வரம்பில் மட்டுமே பாதுகாக்கப்படுகிறது என்பதை கவனத்தில் கொள்ள வேண்டும் α = const. வெப்பநிலை மாற்றங்களின் பெரிய இடைவெளியில், எலக்ட்ரோலைட்டுகளின் எதிர்ப்பின் வெப்பநிலை சார்பு நேரியல் அல்ல. வரைபட ரீதியாக, உலோக கடத்திகள் மற்றும் எலக்ட்ரோலைட்டுகளின் எதிர்ப்பின் வெப்பநிலை சார்பு புள்ளிவிவரங்கள் 1, a, b இல் காட்டப்பட்டுள்ளது. மிகக் குறைந்த வெப்பநிலையில், முழுமையான பூஜ்ஜியத்திற்கு (-273 С С) நெருக்கமாக, பல உலோகங்களின் எதிர்ப்பு திடீரென பூஜ்ஜியத்திற்குக் குறைகிறது. இந்த நிகழ்வு என்று அழைக்கப்படுகிறது மீக்கடத்தல். உலோகம் ஒரு சூப்பர் கண்டக்டிங் நிலைக்கு செல்கிறது. வெப்பநிலையில் உலோக எதிர்ப்பின் சார்பு எதிர்ப்பு வெப்பமானிகளில் பயன்படுத்தப்படுகிறது. வழக்கமாக, ஒரு பிளாட்டினம் கம்பி அத்தகைய வெப்பமானியின் தெர்மோமெட்ரிக் உடலாக எடுக்கப்படுகிறது, வெப்பநிலையின் எதிர்ப்பின் சார்பு போதுமான அளவு ஆய்வு செய்யப்பட்டுள்ளது. வெப்பநிலை மாற்றங்கள் கம்பியின் எதிர்ப்பின் மாற்றத்தால் தீர்மானிக்கப்படுகின்றன, அவற்றை அளவிட முடியும். வழக்கமான திரவ வெப்பமானிகள் பொருத்தமற்றதாக இருக்கும்போது இத்தகைய வெப்பமானிகள் மிகக் குறைந்த மற்றும் மிக உயர்ந்த வெப்பநிலையை அளவிட முடியும். இலக்கியம்உயர்நிலைப் பள்ளியில் அக்செனோவிச் எல்.ஏ. இயற்பியல்: கோட்பாடு. பணிகள். சோதனைகள்: பாடநூல். பொது வழங்கும் நிறுவனங்களுக்கான கொடுப்பனவு. சூழல்கள், கல்வி / எல். ஏ. அக்செனோவிச், என். என். ரக்கினா, கே.எஸ். ஃபரினோ; எட். கே.எஸ்.பரினோ. - எம்.என்: அடுகாட்ஸி ஐ வைகவன்னே, 2004 .-- சி. 256-257. ஒரு சிறந்த படிகத்தில், எலக்ட்ரான்களின் சராசரி இலவச பாதை முடிவிலி, மற்றும் மின்சாரத்திற்கு எதிர்ப்பு பூஜ்ஜியம். இந்த நிலையை உறுதிப்படுத்துவது என்பது வெப்பநிலை முழுமையான பூஜ்ஜியத்தை நெருங்கும் போது தூய வருடாந்திர உலோகங்களின் எதிர்ப்பு பூஜ்ஜியமாக இருக்கும் என்பதே. ஒரு இலட்சிய படிக லட்டியில் சுதந்திரமாக நகர்த்துவதற்கான எலக்ட்ரானின் சொத்துக்கு கிளாசிக்கல் இயக்கவியலில் எந்த ஒப்புமையும் இல்லை. சிதறல், எதிர்ப்பின் தோற்றத்திற்கு வழிவகுக்கிறது, லட்டுகளில் கட்டமைப்பு குறைபாடுகள் இருக்கும்போது ஏற்படுகிறது. சிதறல் மையங்களின் அளவு (குறைபாடுகள்) அலைநீளத்தின் கால் பகுதியை தாண்டும்போது பயனுள்ள அலை சிதறல் நிகழ்கிறது என்பது அறியப்படுகிறது. உலோகங்களில், கடத்தல் எலக்ட்ரான்களின் ஆற்றல் 3 - 15 ஈ.வி. இந்த ஆற்றல் 3 - 7 அலைநீளத்திற்கு ஒத்திருக்கிறது. ஆகையால், கட்டமைப்பின் எந்தவொரு நுண்ணிய ஒற்றுமையும் எலக்ட்ரான் அலைகளின் பரவலுக்குத் தடையாக இருக்கிறது மற்றும் பொருளின் எதிர்ப்பின் அதிகரிப்புக்கு காரணமாகிறது. சரியான கட்டமைப்பின் தூய உலோகங்களில், எலக்ட்ரான்களின் சராசரி இலவச பாதையை கட்டுப்படுத்துவதற்கான ஒரே காரணம் படிக லட்டியின் தளங்களில் உள்ள அணுக்களின் வெப்ப அதிர்வு. வெப்ப காரணி காரணமாக உலோகத்தின் மின் எதிர்ப்பு ρ வெப்பத்தால் குறிக்கப்படுகிறது. வெப்பநிலையை அதிகரிப்பதன் மூலம் அணுக்களின் வெப்ப அதிர்வுகளின் வீச்சுகளும், லட்டியின் கால புலத்தின் தொடர்புடைய ஏற்ற இறக்கங்களும் அதிகரிக்கின்றன என்பது தெளிவாகத் தெரிகிறது. இது, எலக்ட்ரான்களின் சிதறலை மேம்படுத்துகிறது மற்றும் எதிர்ப்பின் அதிகரிப்புக்கு காரணமாகிறது. எதிர்ப்பின் வெப்பநிலை சார்புகளின் தன்மையை தரமான முறையில் நிறுவ, பின்வரும் எளிமைப்படுத்தப்பட்ட மாதிரியைப் பயன்படுத்துகிறோம். சிதறல் தீவிரம் அதிர்வுறும் அணுவால் ஆக்கிரமிக்கப்பட்டுள்ள கோள அளவின் குறுக்குவெட்டுக்கு நேரடியாக விகிதாசாரமாகும், மேலும் குறுக்கு வெட்டு பகுதி வெப்ப அதிர்வுகளின் வீச்சின் சதுரத்திற்கு விகிதாசாரமாகும். லட்டு தளத்திலிருந்து ∆а by ஆல் திசைதிருப்பப்பட்ட ஒரு அணுவின் ஆற்றல் வெளிப்பாடு மூலம் தீர்மானிக்கப்படுகிறது
ktr என்பது மீள் பிணைப்பு குணகம் ஆகும், இது அணுவை சமநிலை நிலைக்குத் திருப்புகிறது. கிளாசிக்கல் புள்ளிவிவரங்களின்படி, ஒரு பரிமாண ஹார்மோனிக் ஆஸிலேட்டரின் (ஊசலாடும் அணு) சராசரி ஆற்றல் kT க்கு சமம். இந்த அடிப்படையில், நாங்கள் பின்வரும் சமத்துவத்தை எழுதுகிறோம்:
N அணுக்களின் எலக்ட்ரான்களின் சராசரி இலவச பாதை வெப்பநிலைக்கு நேர்மாறான விகிதாசாரமானது என்பதை நிரூபிப்பது எளிது:
இதன் விளைவாக வரும் விகிதம் குறைந்த வெப்பநிலையில் திருப்தி அடையவில்லை என்பதை கவனத்தில் கொள்ள வேண்டும். உண்மை என்னவென்றால், வெப்பநிலை குறைவதால் அணுக்களின் வெப்ப அதிர்வுகளின் வீச்சுகள் மட்டுமல்லாமல், அதிர்வுகளின் அதிர்வெண்களும் குறையக்கூடும். எனவே, குறைந்த வெப்பநிலையில், லட்டு தளங்களின் வெப்ப அதிர்வுகளால் எலக்ட்ரான் சிதறல் பயனற்றதாகிவிடும். ஊசலாடும் அணுவுடன் எலக்ட்ரானின் தொடர்பு எலக்ட்ரானின் வேகத்தை சற்று மாற்றும். லட்டு அணுக்களின் அதிர்வுகளின் கோட்பாட்டில், வெப்பநிலை ஒரு குறிப்பிட்ட பண்பு வெப்பநிலையுடன் ஒப்பிடும்போது மதிப்பிடப்படுகிறது, இது டெபி வெப்பநிலை ΘD என அழைக்கப்படுகிறது. ஒரு படிகத்தில் உற்சாகப்படுத்தக்கூடிய வெப்ப அதிர்வுகளின் அதிகபட்ச அதிர்வெண்ணை டெபி வெப்பநிலை தீர்மானிக்கிறது:
இந்த வெப்பநிலை படிக லட்டுகளின் முனைகளுக்கு இடையிலான பிணைப்பு சக்திகளைப் பொறுத்தது மற்றும் இது ஒரு திடத்தின் முக்கியமான அளவுருவாகும். டி For க்கு டி உலோகங்களின் எதிர்ப்பானது வெப்பநிலையுடன் நேரியல் மாறுபடும் (படம் 6, பிரிவு III). சோதனை காண்பித்தபடி, வெப்பநிலை சார்பு T (T) இன் நேரியல் தோராயமும் (2/3) of வரிசையின் வெப்பநிலை வரை செல்லுபடியாகும். டிபிழை 10% ஐ தாண்டாது. பெரும்பாலான உலோகங்களுக்கு, டெபி வெப்பநிலை 400 - 450 K ஐ விட அதிகமாக இருக்காது. எனவே, நேரியல் தோராயமானது பொதுவாக அறை வெப்பநிலை மற்றும் அதற்கு மேற்பட்ட வெப்பநிலைகளில் செல்லுபடியாகும். குறைந்த வெப்பநிலை பகுதியில் (T டி), வெப்ப அதிர்வுகளின் (ஃபோனான்கள்) மேலும் மேலும் புதிய அதிர்வெண்களை படிப்படியாக நீக்குவதன் காரணமாக எதிர்ப்பின் குறைவு ஏற்படுகிறது, கோட்பாடு ஒரு சக்தி-சட்ட சார்பு 5 ஐ முன்னறிவிக்கிறது. இயற்பியலில், இந்த விகிதம் ப்ளொச்-க்ரூனிசென் சட்டம் என்று அழைக்கப்படுகிறது. கூர்மையான சக்தி சட்டம் т (Т) இருக்கும் வெப்பநிலை வரம்பு பொதுவாக மிகவும் சிறியது, மற்றும் அடுக்கின் சோதனை மதிப்புகள் 4 முதல் 6 வரை இருக்கும். ஒரு குறுகிய பிராந்தியத்தில், பல கெல்வின் அடங்கிய, பல உலோகங்களில் சூப்பர் கண்டக்டிவிட்டி நிலை ஏற்படலாம் (கீழே காண்க) மற்றும் இந்த எண்ணிக்கை டி எஸ்.வி வெப்பநிலையில் எதிர்ப்பின் தாக்கத்தைக் காட்டுகிறது. சரியான கட்டமைப்பின் தூய உலோகங்களில், வெப்பநிலை சரியாக இருக்கும்போது, எதிர்ப்பும் 0 (கோடு வளைவு) ஆக இருக்கும், மேலும் சராசரி இலவச பாதை முடிவிலிக்கு முனைகிறது. சாதாரண வெப்பநிலையில் கூட, உலோகங்களில் எலக்ட்ரான்களின் சராசரி இலவச பாதை அணுக்களுக்கு இடையிலான தூரத்தை விட நூற்றுக்கணக்கான மடங்கு அதிகமாகும் (அட்டவணை 2).
படம் 6 - ஒரு பரந்த வெப்பநிலை வரம்பில் வெப்பநிலையில் ஒரு உலோக கடத்தியின் எதிர்ப்பின் சார்பு: a, b, c - பல்வேறு உருகிய உலோகங்களின் எதிர்ப்பின் மாறுபாடுகள் அட்டவணை 2 - பல உலோகங்களுக்கு 0 ° C இல் எலக்ட்ரான்களின் சராசரி இலவச பாதை இடைநிலை பகுதி II க்குள், மின்தடை ρ (T) வேகமாக அதிகரிக்கிறது, அங்கு n 5 வரை இருக்கக்கூடும் மற்றும் T = at இல் temperature முதல் 1 வரை வெப்பநிலை அதிகரிப்பதன் மூலம் படிப்படியாக குறைகிறது. டி. பெரும்பாலான உலோகங்களுக்கான வெப்பநிலை சார்பு (T) இல் உள்ள நேரியல் பிரிவு (பகுதி III) உருகும் இடத்திற்கு நெருக்கமான வெப்பநிலைகளுக்கு நீண்டுள்ளது. இந்த விதிக்கு விதிவிலக்கு ஃபெரோ காந்த உலோகங்கள் ஆகும், இதில் ஸ்பின் கோளாறு மூலம் எலக்ட்ரான்களை கூடுதல் சிதறல் நடைபெறுகிறது. உருகும் இடத்திற்கு அருகில், அதாவது. பிராந்திய IV இல், இதன் ஆரம்பம் படம் 6 இல் வெப்பநிலை T nl ஆல் குறிக்கப்படுகிறது, மற்றும் சாதாரண உலோகங்களில், நேரியல் சார்புகளிலிருந்து சில விலகல்களைக் காணலாம். திடப்பொருளிலிருந்து திரவத்திற்கு மாறும்போது, பெரும்பாலான உலோகங்கள் ஏறக்குறைய 1.5 முதல் 2 மடங்கு எதிர்ப்பை அதிகரிப்பதை வெளிப்படுத்துகின்றன, இருப்பினும் அசாதாரண நிகழ்வுகள் உள்ளன: பிஸ்மத் மற்றும் காலியம் போன்ற சிக்கலான படிக அமைப்புகளைக் கொண்ட பொருட்களுக்கு, உருகுவதோடு in குறைவு ஏற்படுகிறது. சோதனை பின்வரும் வடிவத்தை வெளிப்படுத்துகிறது: உலோகத்தை உருகுவது அளவின் அதிகரிப்புடன் இருந்தால், எதிர்ப்பு சக்தி படிப்படியாக அதிகரிக்கிறது; அளவின் எதிர் மாற்றத்துடன் உலோகங்களுக்கு, ρ குறைகிறது. உருகும்போது, இலவச எலக்ட்ரான்களின் எண்ணிக்கையிலோ அல்லது அவற்றின் தொடர்புகளின் தன்மையிலோ குறிப்பிடத்தக்க மாற்றங்கள் எதுவும் இல்லை. In இன் மாற்றத்தின் மீதான தீர்க்கமான செல்வாக்கு செயல்முறைகளை சீர்குலைப்பதன் மூலமும், அணுக்களின் ஏற்பாட்டில் மேலும் ஒழுங்கை மீறுவதன் மூலமும் செலுத்தப்படுகிறது. சில உலோகங்களின் (Ga, Bi) நடத்தையில் காணப்படும் முரண்பாடுகள் இந்த பொருட்களின் உருகும்போது அமுக்கக்கூடிய மாடுலஸின் அதிகரிப்பு மூலம் விளக்கப்படலாம், இது அணுக்களின் வெப்ப அதிர்வுகளின் வீச்சு குறைவோடு இருக்க வேண்டும். ஒரு கெல்வின் (டிகிரி) வெப்பநிலை மாற்றத்துடன் எதிர்ப்பின் ஒப்பீட்டு மாற்றம் எதிர்ப்பின் வெப்பநிலை குணகம் என்று அழைக்கப்படுகிறது:
புள்ளியின் அருகிலுள்ள எதிர்ப்பானது அதிகரிக்கும் வெப்பநிலையுடன் அதிகரிக்கும் போது α of இன் நேர்மறையான அடையாளம் வழக்குக்கு ஒத்திருக்கிறது. Ρ The அளவு வெப்பநிலையின் செயல்பாடாகும். நேரியல் சார்பு ρ (Т) பகுதியில், வெளிப்பாடு இங்கு ρ 0 மற்றும் α ρ ஆகியவை எதிர்ப்பின் எதிர்ப்பின்மை மற்றும் வெப்பநிலை குணகம் ஆகும், இது வெப்பநிலை வரம்பின் தொடக்கத்தைக் குறிக்கிறது, அதாவது. வெப்பநிலை T0; Temperature வெப்பநிலையில் டி. எதிர்ப்பு மற்றும் எதிர்ப்பின் வெப்பநிலை குணகங்களுக்கிடையிலான உறவு பின்வருமாறு:
இங்கு resistance 0 என்பது இந்த மின்தடையின் எதிர்ப்பின் வெப்பநிலை குணகம்; α 1 - எதிர்ப்பு உறுப்பு பொருளின் விரிவாக்கத்தின் வெப்பநிலை குணகம். தூய உலோகங்களுக்கு, α \u003e\u003e α 1; எனவே, அவை α ρ≈ α ஆர். இருப்பினும், தெர்மோஸ்டபிள் உலோக உலோகக் கலவைகளுக்கு, இந்த தோராயமானது நியாயமற்றது. 3 உலோகங்களின் எதிர்ப்பின் மீது அசுத்தங்கள் மற்றும் பிற கட்டமைப்பு குறைபாடுகளின் விளைவு குறிப்பிட்டுள்ளபடி, ஒரு உலோகத்தில் எலக்ட்ரான் அலைகள் சிதறப்படுவதற்கான காரணங்கள் லட்டு தளங்களின் வெப்ப அதிர்வுகள் மட்டுமல்ல, நிலையான கட்டமைப்பு குறைபாடுகளும் ஆகும், அவை படிகத்தின் சாத்தியமான புலத்தின் கால இடைவெளியை மீறுகின்றன. நிலையான கட்டமைப்பு குறைபாடுகளால் சிதறல் வெப்பநிலை சுயாதீனமானது. ஆகையால், வெப்பநிலை முழுமையான பூஜ்ஜியத்தை நெருங்குகையில், உண்மையான உலோகங்களின் எதிர்ப்பு சில நிலையான மதிப்புக்கு முனைகிறது, இது எஞ்சிய எதிர்ப்பு (படம் 6) என்று அழைக்கப்படுகிறது. இது எதிர்ப்பின் சேர்க்கை குறித்த மாட்டிசென் விதியைக் குறிக்கிறது:
அதாவது ஒரு உலோகத்தின் மொத்த எதிர்ப்புத்திறன் என்பது படிக லட்டுகளின் முனைகளின் வெப்ப அதிர்வுகளால் எலக்ட்ரான்கள் சிதறல் மற்றும் நிலையான கட்டமைப்பு குறைபாடுகளால் எலக்ட்ரான்களை சிதறடிப்பதன் காரணமாக எஞ்சியிருக்கும் எதிர்ப்பு சக்தி ஆகியவற்றின் எதிர்ப்பின் கூட்டுத்தொகையாகும். இந்த விதிக்கு விதிவிலக்கு என்பது சூப்பர் கண்டக்டிங் உலோகங்கள், இதில் எதிர்ப்பு ஒரு குறிப்பிட்ட வெப்பநிலைக்குக் கீழே மறைந்துவிடும். எஞ்சிய எதிர்ப்பிற்கு மிக முக்கியமான பங்களிப்பு அசுத்தங்களால் சிதறடிக்கப்படுவதன் மூலம் செய்யப்படுகிறது, அவை எப்போதும் ஒரு உண்மையான கடத்தியில் மாசுபாடாகவோ அல்லது கலப்பு (அதாவது, வேண்டுமென்றே அறிமுகப்படுத்தப்பட்ட) உறுப்புகளாகவோ இருக்கின்றன. எந்தவொரு தூய்மையற்ற சேர்க்கையும் அடிப்படை உலோகத்துடன் ஒப்பிடும்போது அதிகரித்த கடத்துத்திறனைக் கொண்டிருந்தாலும் இன் அதிகரிப்புக்கு வழிவகுக்கிறது என்பதை கவனத்தில் கொள்ள வேண்டும். எனவே, 0.01 இல் அறிமுகம். வெள்ளி அசுத்தங்களின் விகிதம் தாமிரத்தின் எதிர்ப்பை 0.002 μm ஓம் மீ அதிகரிக்கிறது. அசுத்தங்களின் குறைந்த உள்ளடக்கத்தில், தூய்மையற்ற அணுக்களின் செறிவுக்கு விகிதாச்சாரத்தில் எதிர்ப்பு சக்தி அதிகரிக்கிறது என்பது சோதனை ரீதியாக நிறுவப்பட்டது. படம் 7 மேட்டிசென் விதியை விளக்குகிறது, இது தூய செம்பு மற்றும் அதன் உலோகக் கலவைகளின் எதிர்ப்பின் வெப்பநிலை சார்புகளை ஒரு சிறிய அளவுடன் (சுமார் 4 மணிக்கு.% வரை) இண்டியம், ஆண்டிமனி, தகரம் மற்றும் ஆர்சனிக் ஆகியவை பரஸ்பரம் இணையாக இருப்பதைக் காட்டுகிறது.
படம் 7 - மேட்டிசென் விதியை விளக்கும் திட தீர்வுகளின் வகையின் செப்பு உலோகக்கலவைகளின் எதிர்ப்பின் வெப்பநிலை சார்பு: 1 - தூய கியூ; 2 - Cu - 1.03 at.% In; 3 - Cu - 1.12 at.% Nl உலோகக் கடத்திகளின் எஞ்சிய எதிர்ப்பில் வெவ்வேறு அசுத்தங்கள் வெவ்வேறு விளைவுகளை ஏற்படுத்துகின்றன. தூய்மையற்ற சிதறலின் செயல்திறன் லட்டியில் உள்ள குழப்பமான ஆற்றலால் தீர்மானிக்கப்படுகிறது, இதன் மதிப்பு அதிகமாக உள்ளது, தூய்மையற்ற அணுக்களுக்கும் உலோகத்திற்கும் இடையிலான வேறுபாடு அதிகமானது - கரைப்பான் (அடிப்படை). மோனோவெலண்ட் உலோகங்களைப் பொறுத்தவரை, எஞ்சிய எதிர்ப்பில் 1 இல் மாற்றம்.% தூய்மையற்ற தன்மை (மின் எதிர்ப்பின் "தூய்மையற்ற" குணகம்) லிண்டே விதிக்குக் கீழ்ப்படிகிறது:
a மற்றும் b என்பது உலோகத்தின் தன்மை மற்றும் உறுப்புகளின் கால அமைப்பில் ஒரு தூய்மையற்ற அணு ஆக்கிரமிக்கும் காலத்தைப் பொறுத்து மாறிலிகள்; இசட் - உலோகத்தின் மாறுபாடுகளுக்கு இடையிலான வேறுபாடு - கரைப்பான் மற்றும் தூய்மையற்ற அணு. சூத்திரம் 15 இலிருந்து, உலோகக் கூறுகளின் அசுத்தங்களின் விளைவைக் காட்டிலும் கடத்துத்திறன் குறைவதில் மெட்டல்லாய்டு அசுத்தங்களின் விளைவு வலுவானது என்பதைப் பின்தொடர்கிறது. அசுத்தங்களுக்கு மேலதிகமாக, அவற்றின் சொந்த கட்டமைப்பு குறைபாடுகள் - காலியிடங்கள், இடையிடையேயான அணுக்கள், இடப்பெயர்வுகள் மற்றும் தானிய எல்லைகள் - மீதமுள்ள எதிர்ப்பிற்கு ஒரு குறிப்பிட்ட பங்களிப்பை வழங்குகின்றன. புள்ளி குறைபாடுகளின் செறிவு வெப்பநிலையுடன் அதிவேகமாக அதிகரிக்கிறது மற்றும் உருகும் இடத்திற்கு அருகில் அதிக மதிப்புகளை அடையலாம். கூடுதலாக, ஒரு பொருள் உயர் ஆற்றல் துகள்களுடன் கதிர்வீச்சு செய்யப்படும்போது காலியிடங்கள் மற்றும் இடைநிலை அணுக்கள் எளிதில் எழுகின்றன, எடுத்துக்காட்டாக, ஒரு அணு உலையில் இருந்து நியூட்ரான்கள் அல்லது ஒரு முடுக்கிலிருந்து அயனிகள். அளவிடப்பட்ட எதிர்ப்பு மதிப்பிலிருந்து, ஒருவர் கதிர்வீச்சு சேதத்தின் அளவை தீர்மானிக்க முடியும். அதே வழியில், கதிரியக்க மாதிரியின் குறைப்பை (அனீலிங்) ஒருவர் கண்டுபிடிக்க முடியும். தாமிரத்தின் எஞ்சிய எதிர்ப்பில் 1 இல் மாற்றம்.% புள்ளி குறைபாடுகள்: காலியிடங்களில் 0.010 முதல் 0.015 μOhm ஓம்; இடைநிலை அணுக்களின் விஷயத்தில், 0.005-0.010 μOhm ஓம். எஞ்சிய எதிர்ப்பு என்பது இரசாயன தூய்மை மற்றும் உலோகங்களின் கட்டமைப்பு முழுமையின் மிக முக்கியமான பண்பு. நடைமுறையில், குறிப்பாக அதிக தூய்மையின் உலோகங்களுடன் பணிபுரியும் போது, அசுத்தங்களின் உள்ளடக்கத்தை மதிப்பிடுவதற்கு அறை வெப்பநிலை மற்றும் திரவ ஹீலியம் வெப்பநிலையில் உள்ள எதிர்ப்பின் விகிதம் அளவிடப்படுகிறது:
உலோகத்தை தூய்மையானது, அதிக மதிப்பு. தூய்மையான உலோகங்களில் (தூய்மையின் அளவு 99.99999%), அளவுரு 10 10 5 வரிசையின் மதிப்பைக் கொண்டுள்ளது. உலோகங்கள் மற்றும் உலோகக் கலவைகளின் எதிர்ப்பின் மீது பெரும் செல்வாக்கு மன அழுத்த நிலையால் ஏற்படும் சிதைவுகளால் செலுத்தப்படுகிறது. இருப்பினும், இந்த செல்வாக்கின் அளவு அழுத்தங்களின் தன்மையால் தீர்மானிக்கப்படுகிறது. எடுத்துக்காட்டாக, பெரும்பாலான உலோகங்களில் விரிவான சுருக்கத்துடன், எதிர்ப்பு சக்தி குறைகிறது. அணுக்களின் அணுகுமுறை மற்றும் லட்டியின் வெப்ப அதிர்வுகளின் வீச்சு குறைவு ஆகியவற்றால் இது விளக்கப்படுகிறது. பிளாஸ்டிக் சிதைவு மற்றும் கடினப்படுத்துதல் எப்போதும் உலோகங்கள் மற்றும் உலோகக் கலவைகளின் எதிர்ப்பை அதிகரிக்கும். இருப்பினும், இந்த அதிகரிப்பு, தூய உலோகங்களின் குறிப்பிடத்தக்க கடினப்படுத்தலுடன் கூட, ஒரு சில சதவீதமாகும். வெப்பத்தைத் தணிப்பது in இன் அதிகரிப்புக்கு வழிவகுக்கிறது, இது லட்டு சிதைவுகள் மற்றும் உள் அழுத்தங்களின் தோற்றத்துடன் தொடர்புடையது. வெப்ப சிகிச்சை (அனீலிங்) மூலம் மறுகட்டமைப்பின் போது, குறைபாடுகள் குணமடைந்து உள் அழுத்தங்கள் நிவாரணம் பெறுவதால், எதிர்ப்பை அதன் அசல் மதிப்பிற்குக் குறைக்கலாம். திடமான தீர்வுகளின் தனித்தன்மை என்னவென்றால், ost கணிசமாக (பல மடங்கு) வெப்பக் கூறுகளை மீறலாம். பல இரண்டு-கூறு கலவைகளுக்கு, கலவையைப் பொறுத்து ost ost இன் மாற்றம் படிவத்தின் பரவளைய சார்பு மூலம் நன்கு விவரிக்கப்படுகிறது சி என்பது அலாய் தன்மையைப் பொறுத்து ஒரு மாறிலி; x a மற்றும் x in ஆகியவை அலாய் உள்ள கூறுகளின் அணு பின்னங்கள் ஆகும். 16 என்ற விகிதம் நோர்தெய்மின் சட்டம் என்று அழைக்கப்பட்டது. பைனரி ஏ - பி திட தீர்வுகளில், பி அணுக்கள் உலோகம் A (திட தீர்வு ) மற்றும் ஒரு அணுக்கள் உலோக B (திட தீர்வு ) உடன் சேர்க்கப்படும்போது மீதமுள்ள எதிர்ப்பு இரண்டையும் அதிகரிக்கிறது, மேலும் இந்த மாற்றம் ஒரு சமச்சீர் வளைவால் வகைப்படுத்தப்படுகிறது . தொடர்ச்சியான திடமான தீர்வுகளில், எதிர்ப்புத்திறன் அதிகமாக உள்ளது, கலவையில் தூய்மையான கூறுகளிலிருந்து அலாய் பிரிக்கப்படுகிறது. மீதமுள்ள எதிர்ப்பு ஒவ்வொரு கூறுகளின் சமமான உள்ளடக்கத்துடன் அதன் அதிகபட்ச மதிப்பை அடைகிறது (x a = x in = 0.5). கலவையின் மாற்றத்துடன் கட்ட மாற்றங்கள் கவனிக்கப்படாவிட்டால், தொடர்ச்சியான திட தீர்வுகளின் எதிர்ப்பின் மாற்றத்தை நார்தெய்ம் சட்டம் மிகவும் துல்லியமாக விவரிக்கிறது மற்றும் அவற்றின் கூறுகள் எதுவும் மாற்றம் அல்லது அரிய-பூமி கூறுகளில் இல்லை. அத்தகைய அமைப்புகளுக்கு ஒரு எடுத்துக்காட்டு Au - Ag, Cu - Ag, Cu - Au, W - Mo, போன்ற உலோகக்கலவைகள். திட தீர்வுகள், மாற்றுக் குழுவின் உலோகங்களான கூறுகள் சற்றே வித்தியாசமாக செயல்படுகின்றன (படம் 8). இந்த வழக்கில், உயர் கூறு செறிவுகளில், கணிசமாக பெரிய எஞ்சிய எதிர்ப்பு காணப்படுகிறது, இது வேலன்ஸ் எலக்ட்ரான்களின் ஒரு பகுதியை உள் நிரப்பப்படாத டி - மாற்றம் உலோக அணுக்களின் குண்டுகளுக்கு மாற்றுவதோடு தொடர்புடையது. கூடுதலாக, அத்தகைய உலோகக்கலவைகளில், அதிகபட்சம் பெரும்பாலும் 50% தவிர மற்ற செறிவுகளுக்கு ஒத்திருக்கிறது.
படம் 8 - கூறுகளின் சதவீதத்தில் செப்பு-நிக்கல் உலோகக் கலவைகளின் எதிர்ப்பின் சார்பு (1) மற்றும் எதிர்ப்பின் வெப்பநிலை குணகம் (2) அலாய் அதிக எதிர்ப்பைக் கொண்டால், அதன் α lower குறைவாக இருக்கும். திடமான தீர்வுகளில், ost, ஒரு விதியாக, கணிசமாக t ஐ விட அதிகமாக உள்ளது மற்றும் வெப்பநிலையைப் பொறுத்தது அல்ல. வெப்பநிலை குணகத்தின் வரையறையின்படி
Metals pure தூய உலோகங்கள் ஒருவருக்கொருவர் சற்று வித்தியாசமாக இருப்பதைக் கருத்தில் கொண்டு, வெளிப்பாடு 17 ஐ எளிதாக பின்வரும் வடிவத்திற்கு மாற்றலாம்:
செறிவூட்டப்பட்ட திடக் கரைசல்களில், ost என்பது பொதுவாக ஒரு வரிசை அல்லது ρ t ஐ விட அதிகமாக இருக்கும். எனவே, ρ ρ spl தூய உலோகத்தை விட கணிசமாகக் குறைவாக இருக்கலாம். தெர்மோஸ்டபிள் கடத்தும் பொருட்களைப் பெறுவதற்கான அடிப்படை இது. பல சந்தர்ப்பங்களில், உலோகக் கலவைகளின் எதிர்ப்பின் வெப்பநிலை சார்பு ஒரு எளிய சேர்க்கை வழக்கமான தன்மையைக் காட்டிலும் சிக்கலானதாக மாறும். அலாய்ஸின் எதிர்ப்பின் வெப்பநிலை குணகம் விகிதம் 18 ஆல் கணிக்கப்பட்டதை விட கணிசமாகக் குறைவாக இருக்கலாம். குறிப்பிடப்பட்ட முரண்பாடுகள் தாமிர-நிக்கல் உலோகக் கலவைகளில் தெளிவாக வெளிப்படுகின்றன (படம் 8). சில உலோகக் கலவைகளில், கூறுகளின் சில விகிதங்களில், எதிர்மறை α observed காணப்படுகிறது (மாறிலிக்கு). அலாய் கூறுகளின் சதவீதத்திலிருந்து ρ மற்றும் α in இல் இதுபோன்ற மாற்றம், தூய்மையான உலோகங்களுடன் ஒப்பிடும்போது, மிகவும் சிக்கலான கலவை மற்றும் கட்டமைப்பைக் கொண்டு, உலோகக் கலவைகளை கிளாசிக்கல் உலோகங்களாகக் கருத முடியாது என்பதன் மூலம் விளக்க முடியும். அவற்றின் கடத்துத்திறனில் மாற்றம் இலவச எலக்ட்ரான்களின் சராசரி இலவச பாதையில் ஏற்பட்ட மாற்றத்தால் மட்டுமல்ல, சில சந்தர்ப்பங்களில், அதிகரிக்கும் வெப்பநிலையுடன் சார்ஜ் கேரியர்களின் செறிவில் ஓரளவு அதிகரிப்பால் ஏற்படுகிறது. அதிகரிக்கும் வெப்பநிலையுடன் சராசரி இலவச பாதையில் குறைவு சார்ஜ் கேரியர்களின் செறிவு அதிகரிப்பால் ஈடுசெய்யப்படும் ஒரு அலாய், பூஜ்ஜிய வெப்பநிலை குணகம் எதிர்ப்பின் தன்மையைக் கொண்டுள்ளது. நீர்த்த கரைசல்களில், ஒரு கூறு (எடுத்துக்காட்டாக, கூறு B) மிகக் குறைந்த செறிவால் வகைப்படுத்தப்பட்டு, தூய்மையற்றதாகக் கருதப்படலாம், சூத்திரம் 16 இல் துல்லியத்தை இழக்காமல் ஒருவர் (1-x இன்) 1 வைக்கலாம். மீதமுள்ள எதிர்ப்பிற்கும் உலோகத்தில் உள்ள தூய்மையற்ற அணுக்களின் செறிவுக்கும் இடையே ஒரு நேரியல் உறவுக்கு வருகிறோம்:
நிலையான சி எஞ்சிய எதிர்ப்பின் மாற்றங்களை ost 1 இல்.% தூய்மையற்ற தன்மையைக் குறிக்கிறது. சில உலோகக்கலவைகள் அவற்றின் உற்பத்தியின் போது கலவையில் சில விகிதாச்சாரங்கள் பராமரிக்கப்படுமானால் கட்டளையிடப்பட்ட கட்டமைப்புகளை உருவாக்குகின்றன. வரிசைப்படுத்துவதற்கான காரணம் ஒரே மாதிரியான அணுக்களுடன் ஒப்பிடும்போது வேறுபட்ட அணுக்களின் வலுவான வேதியியல் தொடர்பு. இந்த கட்டமைப்பு ஒரு குறிப்பிட்ட சிறப்பியல்பு வெப்பநிலை T cr க்கு கீழே கட்டளையிடப்பட்டுள்ளது, இது முக்கியமான வெப்பநிலை (அல்லது குர்னகோவ் வெப்பநிலை) என அழைக்கப்படுகிறது. எடுத்துக்காட்டாக, 50 இல் கொண்ட அலாய். % Cu மற்றும் 50 இல். % Zn ( - பித்தளை) உடலை மையமாகக் கொண்ட கன அமைப்பைக் கொண்டுள்ளது. T 360C இல், தாமிர மற்றும் துத்தநாக அணுக்கள் தோராயமாக மற்றும் புள்ளிவிவர ரீதியாக லட்டு தளங்களில் விநியோகிக்கப்படுகின்றன. திடப்பொருட்களின் மின் எதிர்ப்பின் காரணம் லட்டு அணுக்களுடன் இலவச எலக்ட்ரான்களின் மோதல் அல்ல, ஆனால் அவை மொழிபெயர்ப்பு சமச்சீர்மை மீறலுக்கு காரணமான கட்டமைப்பு குறைபாடுகளில் சிதறடிக்கப்படுகின்றன. ஒரு திடமான தீர்வை வரிசைப்படுத்தும் போது, லட்டியின் அணு கலவையின் மின்காந்த புலத்தின் காலநிலை மீட்டமைக்கப்படுகிறது, இதன் மூலம் எலக்ட்ரான் சராசரி இலவச பாதையை அதிகரிக்கிறது மற்றும் அலாய் மைக்ரோஹீட்டோரோஜெனிட்டி மூலம் சிதறல் காரணமாக கூடுதல் எதிர்ப்பு முற்றிலும் மறைந்துவிடும். குறிப்பிட்ட மேற்பரப்பு எதிர்ப்பு மற்றும் அதன் வெப்பநிலை குணகம் ஆகியவற்றில் உலோகப் படங்களின் தடிமன் விளைவு ஒருங்கிணைந்த சுற்றுகள் தயாரிப்பில், உலோகத் திரைப்படங்கள் இடை-உறுப்பு இணைப்புகள், தொடர்பு பட்டைகள், மின்தேக்கி தகடுகள், தூண்டல், காந்த மற்றும் எதிர்ப்பு கூறுகளுக்குப் பயன்படுத்தப்படுகின்றன. படங்களின் அமைப்பு, மின்தேக்கத்தின் நிலைமைகளைப் பொறுத்து, உருவமற்ற மின்தேக்கி முதல் எபிடாக்சியல் படங்கள் வரை மாறுபடும் - ஒரு சரியான ஒற்றை-படிக அடுக்கின் கட்டமைப்புகள். கூடுதலாக, உலோக படங்களின் பண்புகள் அளவு விளைவுகளுடன் தொடர்புடையவை. எனவே பட தடிமன் எல் சி.எஃப் உடன் ஒப்பிடப்பட்டால் அவற்றின் மின் கடத்துத்திறன் பங்களிப்பு குறிப்பிடத்தக்கதாகும். படம் 9 மெல்லிய படங்களின் மேற்பரப்பு எதிர்ப்பின் வழக்கமான சார்புகளையும் அதன் தடிமன் மீது அதன் வெப்பநிலை குணகத்தையும் காட்டுகிறது. கட்டமைப்பு (நீளம் எல், அகலம் பி, பட தடிமன் எச்) மற்றும் தொழில்நுட்ப உறவு என்பதால் () மெல்லிய பட மின்தடையின் (TPR) அளவுருக்கள் சமன்பாட்டால் அமைக்கப்படுகின்றன:
இங்கு ρ s = ρ / h என்பது சதுர எதிர்ப்பு (அல்லது குறிப்பிட்ட மேற்பரப்பு எதிர்ப்பு), பின்னர் நாம் ρ s க்கு பதிலாக பாரம்பரிய குறியீட்டையும் s க்கு பதிலாக ஐ எடுத்துக்கொள்கிறோம்.
படம் 9- படத்தின் தடிமன் from change மற்றும் the மாற்றத்தின் தன்மை h உலோகப் படங்களின் வளர்ச்சி நான்கு நிலைகளுடன் உள்ளது: நான் - உலோக தீவுகளின் உருவாக்கம் மற்றும் வளர்ச்சி (கட்டணம் பரிமாற்றத்திற்கு பொறுப்பான வழிமுறைகள், - ஃபெர்மி மட்டத்திற்கு மேலே அமைந்துள்ள எலக்ட்ரான்களின் தெர்மோனிக் உமிழ்வு மற்றும் சுரங்கப்பாதை. உலோகத் திரைப்படம் இல்லாத அடி மூலக்கூறின் பகுதிகளின் மேற்பரப்பு எதிர்ப்பு அதிகரிக்கும் வெப்பநிலையுடன் குறைகிறது, இது எதிர்மறை small small சிறிய தடிமன் படங்களை ஏற்படுத்துகிறது ); II - தங்களுக்கு இடையேயான தீவுகளின் தொடுதல் (y of of இன் அடையாளத்தை மாற்றும் தருணம் உலோகத்தின் வகை, திரைப்பட உருவாக்கம் நிலைமைகள், தூய்மையற்ற செறிவு, அடி மூலக்கூறு மேற்பரப்பின் நிலை ஆகியவற்றைப் பொறுத்தது); III - தீவுகளுக்கிடையேயான இடைவெளிகளின் அளவு மற்றும் எண்ணிக்கை குறையும் போது, ஒரு கடத்தும் கண்ணி உருவாக்கம்; IV - தொடர்ச்சியான கடத்தும் திரைப்படத்தின் உருவாக்கம், கடத்துத்திறன் மற்றும் massive large பாரிய கடத்திகளின் மதிப்பை அணுகும்போது, ஆனால் படத்தின் குறிப்பிட்ட எதிர்ப்பானது மொத்த மாதிரியை விட அதிகமாக உள்ளது, அதிக செறிவு குறைபாடுகள் காரணமாக, படத்தில் தேங்கியுள்ள அசுத்தங்கள். ஆகையால், தானிய எல்லைகளுடன் ஆக்ஸிஜனேற்றப்பட்ட படங்கள் உடல் ரீதியாக திடமானவை என்றாலும் அவை மின்சார ரீதியாக நிறுத்தப்படுகின்றன. மேற்பரப்பில் இருந்து பிரதிபலிக்கும்போது எலக்ட்ரான் குறைவதால் of மற்றும் அளவு விளைவு ஆகியவற்றின் பங்களிப்பு இலவச பாதையை குறிக்கிறது. மெல்லிய-பட மின்தடையங்களின் உற்பத்தியில், மூன்று குழுக்கள் பொருட்கள் பயன்படுத்தப்படுகின்றன: உலோகங்கள், உலோக கலவைகள், சான்றிதழ்கள். 5 சூப்பர் கண்டக்டிவிட்டி இயற்பியல் தன்மை சூப்பர் கண்டக்டிவிட்டி நிகழ்வு குவாண்டம் கோட்பாட்டின் மூலம் விளக்கப்படுகிறது, ஒரு உலோகத்தில் எலக்ட்ரான்கள் ஒருவருக்கொருவர் ஈர்க்கப்படும்போது ஏற்படுகிறது. நேர்மறையாக சார்ஜ் செய்யப்பட்ட அயனிகளைக் கொண்ட ஒரு ஊடகத்தில் ஈர்ப்பு சாத்தியமாகும், இதன் புலம் எலக்ட்ரான்களுக்கு இடையில் கூலொம்ப் விரட்டும் சக்திகளை பலவீனப்படுத்துகிறது. மின் கடத்துத்திறனில் பங்கேற்கும் எலக்ட்ரான்கள் மட்டுமே, அதாவது ஃபெர்மி மட்டத்திற்கு அருகில் அமைந்துள்ளது. எதிர் சுழல் கொண்ட எலக்ட்ரான்கள் ஜோடிகளாக பிணைக்கப்பட்டுள்ளன, அவை கூப்பர் என்று அழைக்கப்படுகின்றன. கூப்பர் ஜோடிகளின் உருவாக்கத்தில், வெப்ப லட்டு அதிர்வுகளுடன் எலக்ட்ரான்களின் தொடர்பு மூலம் தீர்க்கமான பங்கு வகிக்கப்படுகிறது - ஃபோனான்கள், இது உறிஞ்சி உருவாக்க முடியும். எலக்ட்ரான்களில் ஒன்று லட்டுடன் தொடர்பு கொள்கிறது - அதை உற்சாகப்படுத்துகிறது மற்றும் அதன் வேகத்தை மாற்றுகிறது; மற்ற எலக்ட்ரான், தொடர்புகொண்டு, அதை ஒரு சாதாரண நிலைக்கு மொழிபெயர்க்கிறது மற்றும் அதன் வேகத்தையும் மாற்றுகிறது. இதன் விளைவாக, லட்டியின் நிலை மாறாது, மற்றும் எலக்ட்ரான்கள் வெப்ப ஆற்றலின் அளவை பரிமாறிக்கொள்கின்றன - ஃபோனான்கள். பரிமாற்ற ஃபோனான் தொடர்பு எலக்ட்ரான்களுக்கு இடையிலான ஈர்ப்பு சக்திகளை ஏற்படுத்துகிறது, இது கூலொம்ப் விரட்டலை மீறுகிறது. ஃபோனான் பரிமாற்றம் தொடர்ந்து நிகழ்கிறது. லட்டு வழியாக நகரும் ஒரு எலக்ட்ரான் அதை துருவப்படுத்துகிறது, அதாவது. அருகிலுள்ள அயனிகளை தனக்கு ஈர்க்கிறது; எலக்ட்ரான் பாதைக்கு அருகில் நேர்மறை கட்டணத்தின் அடர்த்தி அதிகரிக்கிறது. இரண்டாவது எலக்ட்ரான் அதிகப்படியான நேர்மறையான கட்டணத்துடன் ஒரு பகுதியால் ஈர்க்கப்படுகிறது, இதன் விளைவாக, எலக்ட்ரான்களுக்கு இடையிலான லட்டுடன் தொடர்பு கொள்வதால், கவர்ச்சிகரமான சக்திகள் (கூப்பர் ஜோடி) எழுகின்றன. இந்த ஜோடி வடிவங்கள் ஒருவருக்கொருவர் விண்வெளியில் ஒன்றுடன் ஒன்று சேர்ந்து, சிதைந்து மீண்டும் உருவாக்கி, ஒரு எலக்ட்ரான் மின்தேக்கத்தை உருவாக்குகின்றன, இதன் உள் தொடர்பு காரணமாக ஆற்றல் துண்டிக்கப்பட்ட எலக்ட்ரான்களின் மொத்தத்தை விட குறைவாக உள்ளது. ஒரு சூப்பர் கண்டக்டரின் ஆற்றல் ஸ்பெக்ட்ரமில் ஒரு ஆற்றல் இடைவெளி தோன்றுகிறது - தடைசெய்யப்பட்ட ஆற்றல் நிலைகளின் பகுதி. இணைக்கப்பட்ட எலக்ட்ரான்கள் ஆற்றல் இடைவெளியின் அடிப்பகுதியில் அமைந்துள்ளன. ஆற்றல் இடைவெளியின் அளவு வெப்பநிலையைப் பொறுத்தது, முழுமையான பூஜ்ஜியத்தில் அதிகபட்சத்தை அடைகிறது மற்றும் T st இல் முற்றிலும் மறைந்துவிடும். பெரும்பாலான சூப்பர் கண்டக்டர்களுக்கு, ஆற்றல் இடைவெளி 10 -4 - 10 -3 ஈ.வி. எலக்ட்ரான் சிதறல் வெப்ப அதிர்வுகளிலும் அசுத்தங்களிலும் நிகழ்கிறது, ஆனால் உடன் எலக்ட்ரான்களை தரை நிலையிலிருந்து உற்சாகமான நிலைக்கு மாற்றுவதற்கான ஆற்றல் இடைவெளி இருப்பதற்கு போதுமான வெப்ப ஆற்றல் தேவைப்படுகிறது, இது குறைந்த வெப்பநிலையில் இல்லை; எனவே, இணைக்கப்பட்ட எலக்ட்ரான்கள் கட்டமைப்பு குறைபாடுகளில் சிதறவில்லை. கூப்பர் ஜோடிகளின் ஒரு அம்சம் என்னவென்றால், அவர்கள் ஒருவருக்கொருவர் சுயாதீனமாக தங்கள் மாநிலங்களை மாற்ற முடியாது, எலக்ட்ரான் அலைகள் ஒரே நீளம் மற்றும் கட்டத்தைக் கொண்டுள்ளன, அதாவது. அவை கட்டமைப்பின் குறைபாடுகளைச் சுற்றியுள்ள ஒரு ஒற்றை அலையாகக் கருதப்படலாம். முழுமையான பூஜ்ஜியத்தில், அனைத்து எலக்ட்ரான்களும் ஜோடிகளாக இணைக்கப்பட்டுள்ளன, அதிகரிப்புடன், சில ஜோடிகள் உடைந்து இடைவெளியின் அகலம் குறைகிறது, டி ஸ்ட்ரீட்டில் அனைத்து ஜோடிகளும் அழிக்கப்படுகின்றன, இடைவெளியின் அகலம் மறைந்து சூப்பர் கண்டக்டிவிட்டி உடைக்கிறது. சூப்பர் கண்டக்டிங் நிலைக்கு மாற்றம் மிகவும் குறுகிய வெப்பநிலை வரம்பில் நிகழ்கிறது, கட்டமைப்பின் பன்முகத்தன்மை வரம்பின் விரிவாக்கத்தை ஏற்படுத்துகிறது. சூப்பர் கண்டக்டர்களின் மிக முக்கியமான சொத்து - காந்தப்புலம் பொருளின் தடிமனுக்குள் ஊடுருவாது, சக்தியின் கோடுகள் சூப்பர் கண்டக்டரைச் சுற்றிச் செல்கின்றன (மீஸ்னர் விளைவு) - மாதிரியின் உள்ளே இருக்கும் வெளிப்புற புலத்தை முழுவதுமாக ஈடுசெய்யும் சூப்பர் கண்டக்டரின் காந்தப்புலத்தில் ஒரு வட்டக் குறைக்கப்படாத மின்னோட்டம் எழுகிறது. காந்தப்புலத்தின் ஊடுருவலின் ஆழம் 10 -7 - 10 -8 மீ - சூப்பர் கண்டக்டர் ஒரு சிறந்த டயமக்னடிக் ஆகும்; காந்தப்புலத்திலிருந்து வெளியேற்றப்படுகிறது (ஒரு காந்தத்தால் தூண்டப்படும் அழுகாத நீரோட்டங்கள் புழக்கத்தில் இருக்கும் சூப்பர் கண்டக்டிங் பொருளின் வளையத்தின் மீது ஒரு நிரந்தர காந்தத்தை உருவாக்க முடியும்). காந்தப்புல வலிமை H st ஐ விட அதிகமாக இருக்கும்போது சூப்பர் கண்டக்டிவிட்டி நிலை மீறப்படுகிறது. காந்தப்புலத்தின் செயல்பாட்டின் கீழ் பொருளை சூப்பர் கண்டக்டிங் நிலையிலிருந்து சாதாரண மின் கடத்துத்திறன் நிலைக்கு மாற்றுவதன் தன்மையால், முதல் மற்றும் இரண்டாவது வகையான சூப்பர் கண்டக்டர்கள் வேறுபடுகின்றன. முதல் வகையான சூப்பர் கண்டக்டர்களுக்கு, இந்த மாற்றம் திடீரென நிகழ்கிறது, சூப்பர் கண்டக்டர்களுக்கு, மாற்றம் செயல்முறை படிப்படியாக H cj1 - எச் கோர் 2. இடைவெளியில், பொருள் ஒரு பன்முக நிலையில் உள்ளது, இதில் இயல்பான மற்றும் சூப்பர் கண்டக்டிங் கட்டங்கள் ஒன்றிணைகின்றன, காந்தப்புலம் படிப்படியாக சூப்பர் கண்டக்டருக்குள் ஊடுருவுகிறது, மேல் சிக்கலான தீவிரம் வரை பூஜ்ஜிய எதிர்ப்பு பராமரிக்கப்படுகிறது. முக்கியமான தீவிரம் வகை 1 சூப்பர் கண்டக்டர்களுக்கான வெப்பநிலையைப் பொறுத்தது:
வகை 2 சூப்பர் கண்டக்டர்களில், இடைநிலை மாநில பகுதி வெப்பநிலை குறைந்து விரிவடைகிறது. வகை 1 சூப்பர் கண்டக்டர்களுக்கு (வகை 2 மிகவும் சிக்கலானது) - முக்கியமான மதிப்பான I St = 2πHH St (T) ஐ விட அதிகமாக இருந்தால், சூப்பர் கண்டக்டிவிட்டி வழியாக தற்போதைய கடப்பதன் மூலம் சூப்பர் கண்டக்டிவிட்டி உடைக்கப்படலாம். 26 உலோகங்கள் சூப்பர் கண்டக்டிவிட்டி (முக்கியமாக 4.2K க்கும் குறைவான வெப்பநிலைகளைக் கொண்ட 1 வது வகை), 13 கூறுகள் அதிக அழுத்தங்களில் (சிலிக்கான், ஜெர்மானியம், டெல்லூரியம், ஆண்டிமனி) சூப்பர் கண்டக்டிவிட்டி வெளிப்படுத்துகின்றன. தாமிரம், தங்கம், வெள்ளி ஆகியவற்றைக் கொண்டிருக்க வேண்டாம்: குறைந்த எதிர்ப்பு என்பது படிக லட்டுடன் எலக்ட்ரான்களின் பலவீனமான தொடர்பையும், ஃபெரோ மற்றும் ஆண்டிஃபெரோ காந்தங்களிலும் குறிக்கிறது; குறைக்கடத்திகள் டோபண்டுகளின் பெரிய செறிவு சேர்ப்பதன் மூலம் மொழிபெயர்க்கப்படுகின்றன; உயர் மின்கடத்தா மாறிலி (ஃபெரோஎலக்ட்ரிக்ஸ்) கொண்ட மின்கடத்தாவில், எலக்ட்ரான்களுக்கு இடையிலான கூலம்ப் விரட்டும் சக்திகள் பெரிதும் பலவீனமடைகின்றன, மேலும் அவை சூப்பர் கண்டக்டிவிட்டி பண்புகளை வெளிப்படுத்தலாம். இன்டர்மெட்டாலிக் கலவைகள் மற்றும் உலோகக்கலவைகள் வகை 2 சூப்பர் கண்டக்டர்களைச் சேர்ந்தவை, இருப்பினும், இந்த பிரிவு முழுமையானது அல்ல (வகை 1 சூப்பர் கண்டக்டரை நீங்கள் தட்டச்சு குறைபாடுகளின் போதுமான செறிவை உருவாக்கினால் வகை 2 சூப்பர் கண்டக்டராக மாற்றலாம். சூப்பர் கண்டக்டிங் கடத்திகளின் உற்பத்தி தொழில்நுட்பத்துடன் தொடர்புடையது சிரமங்கள் (அவை உடையக்கூடிய தன்மை, குறைந்த வெப்ப கடத்துத்திறன் கொண்டவை), தாமிரத்துடன் ஒரு சூப்பர் கண்டக்டர் கலவையை உருவாக்குகின்றன (ஒரு வெண்கல முறை அல்லது ஒரு திட-கட்ட பரவல் முறை - அழுத்தி வரைதல்; வெப்பமூட்டும் தகரம் வெண்கல கொண்டு தகரம் வெண்கல ஒரு அணி, மெல்லிய நியோபியம் இழைகளைக் கொண்டு நிலையை ஒரு மீக்கடத்தி படம் stanida நியோபியம் அமைக்க) NB ஒரு சிதறுகிறது. சோதனை கேள்விகள் 1 எந்த அளவுருக்கள் உலோகங்களின் மின் கடத்துத்திறனைப் பொறுத்தது. உலோகங்களின் கடத்துத்திறனின் குவாண்டம் கோட்பாட்டில் எலக்ட்ரான்களின் ஆற்றல் விநியோகத்தை எந்த புள்ளிவிவரங்கள் விவரிக்கின்றன. உலோகங்களில் உள்ள ஃபெர்மி ஆற்றலை (ஃபெர்மி நிலை) எது தீர்மானிக்கிறது, அது எதைப் பொறுத்தது. உலோகத்தின் மின் வேதியியல் திறன் என்ன? உலோகத்தில் எலக்ட்ரான்களின் இலவச பாதையை எது தீர்மானிக்கிறது. 6 உலோகக்கலவைகளின் உருவாக்கம். உலோகங்களின் எதிர்ப்பின் மீது குறைபாடுகள் இருப்பது எப்படி. கடத்திகளின் எதிர்ப்பின் வெப்பநிலை சார்புகளை விளக்குங்கள். திடமான தீர்வுகள் மற்றும் இயந்திர கலவைகளின் உலோகக் கலவைகளில் ρ மற்றும் TKS க்கான NSKurnakova வடிவங்கள். மின் எதிர்ப்பின் வெவ்வேறு மதிப்புகளைக் கொண்ட கடத்தும் பொருட்களின் நுட்பத்தில் பயன்பாடு. பயன்பாட்டைப் பொறுத்து பொருட்களுக்கான தேவைகள். 10 சூப்பர் கண்டக்டிவிட்டி நிகழ்வு. சூப்பர் மற்றும் கிரையோ-கடத்திகளின் நோக்கங்கள் 6 ஆய்வக பணிகள் 2. கடத்தும் உலோகக் கலவைகளின் பண்புகள் பற்றிய ஆய்வு குறிக்கோள்: இரண்டு-கூறு உலோகக் கலவைகளின் மின் பண்புகளில் ஏற்படும் மாற்றங்களின் வடிவங்களைப் படிப்பது, அவற்றின் கலவையைப் பொறுத்து. ஆய்வகப் பணியின் முதல் பகுதியில், வெவ்வேறு கட்ட கலவைகளைக் கொண்ட உலோகக் கலவைகளின் இரண்டு குழுக்கள் கருதப்படுகின்றன. முதல் குழுவில் A மற்றும் B கூறுகள் ஒருவருக்கொருவர் வரம்பற்ற முறையில் கரைந்து, படிப்படியாக ஒருவருக்கொருவர் லட்டு தளங்களில் மாற்றி, அலாய் ஒரு தூய்மையான கூறுகளிலிருந்து மற்றொன்றுக்கு தொடர்ச்சியான திட தீர்வுகளை உருவாக்குகின்றன. திட நிலையில் இந்த வகையின் எந்த அலாய் ஒற்றை கட்டமாகும், அதே கலவையின் அதே திடமான தீர்வின் தானியங்களைக் கொண்டுள்ளது. திட தீர்வு உலோகக் கலவைகளுக்கு ஒரு எடுத்துக்காட்டு செப்பு-நிக்கல், கு-நி, ஜெர்மானியம்-சிலிக்கான், ஜீ-சி மற்றும் பிற. இரண்டாவது குழுவில் உலோகக்கலவைகள் உள்ளன, அதன் கூறுகள் நடைமுறையில் ஒருவருக்கொருவர் கரைவதில்லை, ஒவ்வொரு கூறுகளும் அதன் சொந்த தானியத்தை உருவாக்குகின்றன. திட நிலை அலாய் பைபாசிக்; அத்தகைய உலோகக்கலவைகள் இயந்திர கலவைகள் என்று அழைக்கப்படுகின்றன. இயந்திர கலவைகளின் உலோகக் கலவைகளின் எடுத்துக்காட்டுகள் Cu-Ag செப்பு-வெள்ளி அமைப்புகள், Sn-Pb டின்-முன்னணி அமைப்புகள் போன்றவை. இயந்திர கலவைகளின் வகைகளின் கலவைகளின் உருவாக்கத்தின் போது (படம் 10, அ), பண்புகள் நேர்கோட்டுடன் (சேர்க்கையாக) மாறுகின்றன மற்றும் தூய கூறுகளின் பண்புகளின் மதிப்புகளுக்கு இடையிலான சராசரியாகும். திட தீர்வுகளின் வகைகளின் உலோகக் கலவைகளை உருவாக்குவதில் (படம் 10, பி), பண்புகள் அதிகபட்ச மற்றும் குறைந்தபட்ச வளைவுகளில் வேறுபடுகின்றன.
படம் 10 - என்.எஸ். குர்னகோவின் வடிவங்கள். உலோகக் கலவைகளின் கட்ட கலவைக்கும் அதன் பண்புகளுக்கும் இடையிலான உறவு உலோகங்கள் மற்றும் உலோகக் கலவைகளின் முக்கிய மின் பண்புகள்: மின் எதிர்ப்பு ivity, hohm; எதிர்ப்பின் வெப்பநிலை குணகம் TKS, பட்டம் -1. வரையறுக்கப்பட்ட நீளத்தின் கடத்தியின் எதிர்ப்பு
கடத்தி பொருட்களின் எதிர்ப்பு சக்தி சிறியது மற்றும் 0.016-10 μOm.m. வரம்பில் உள்ளது. பல்வேறு உலோகக் கடத்திகளின் மின் எதிர்ப்பு சக்தி முக்கியமாக ஒரு குறிப்பிட்ட கடத்தியில் ஒரு எலக்ட்ரானின் சராசரி சராசரி இலவச பாதையைப் பொறுத்தது:
இங்கு µ = 1 / the என்பது எலக்ட்ரான் சிதறல் குணகம். உலோகங்கள் மற்றும் உலோகக்கலவைகளில் உள்ள மின்முனைகளின் திசை இயக்கத்தில் சிதறல் காரணிகள் லட்டு தளங்களில் அமைந்துள்ள நேர்மறை அயனிகள். நேர்மறை அயனிகள் தொடர்ந்து விண்வெளியில் அமைக்கப்பட்டிருக்கும் மிகவும் வழக்கமான, பட்டியலிடப்படாத படிக லட்டு கொண்ட தூய உலோகங்களில், எலக்ட்ரான்களின் சிதறல் சிறியது மற்றும் முக்கியமாக லட்டு தளங்களில் அயனியின் அலைவுகளின் வீச்சால் தீர்மானிக்கப்படுகிறது; தூய உலோகங்களுக்கு ρ≈ A warm warm சூடாக இருக்கும். எங்கே warm சூடாக இருக்கிறது - லட்டு வெப்ப அதிர்வுகளில் எலக்ட்ரான் சிதறல் குணகம். இந்த எலக்ட்ரான் சிதறல் பொறிமுறையானது லாட்டீஸ் வெப்ப அதிர்வுகளில் ஃபோனான் சிதறல் என்று அழைக்கப்படுகிறது. வெப்பநிலை T இன் அதிகரிப்புடன், லட்டு தளங்களில் நேர்மறை அயனிகளின் அலைவுகளின் வீச்சு அதிகரிக்கிறது, புலத்தின் செயல்பாட்டின் கீழ் திசையில் நகரும் எலக்ட்ரான்களின் சிதறல் அதிகரிக்கிறது, சராசரி இலவச பாதை λ குறைகிறது, மற்றும் எதிர்ப்பு அதிகரிக்கிறது. வெப்பநிலை ஒரு டிகிரி மாறும்போது பொருள் எதிர்ப்பின் வளர்ச்சியை மதிப்பிடும் மதிப்பு TCS இன் மின் எதிர்ப்பின் வெப்பநிலை குணகம் என்று அழைக்கப்படுகிறது:
அங்கு R 1 - மாதிரியின் எதிர்ப்பு, வெப்பநிலை T 1 இல் அளவிடப்படுகிறது; ஆர் 2 - அதே மாதிரியின் எதிர்ப்பு, வெப்பநிலை T 2 இல் அளவிடப்படுகிறது. உலோகக் கலவைகளின் இரண்டு அமைப்புகளை நாங்கள் படிக்கிறோம்: கியூ-நி அமைப்பு, அங்கு உலோகக் கலவைகளின் கூறுகள் (தாமிரம் மற்றும் நிக்கல்) ஒருவருக்கொருவர் வரம்பற்ற கரைதிறனின் அனைத்து நிலைகளையும் திட நிலையில் பூர்த்தி செய்கின்றன, எனவே படிகமயமாக்கலின் முடிவில் இந்த அமைப்பில் உள்ள எந்த உலோகக் கலவைகளும் ஒற்றை-கட்ட திட தீர்வாக இருக்கும் (படம் 10, a), மற்றும் Cu-Ag அமைப்பு, அதன் கூறுகள் (தாமிரம் மற்றும் வெள்ளி) வரம்பற்ற கரைதிறனின் நிலைமைகளை பூர்த்தி செய்யாது, அவற்றின் கரைதிறன் அதிக வெப்பநிலையில் கூட சிறியது (10% ஐ தாண்டாது), மற்றும் 300 0 C க்கும் குறைவான வெப்பநிலையில் அதைக் கருத்தில் கொள்ளலாம் கள், அது வரவில்லை, மேலும் எந்த அலாய் செம்பு மற்றும் வெள்ளி தானியங்கள் ஒரு இயந்திர கலவையை கொண்டுள்ளது (படம் 10b). திட தீர்வுகளுக்கு வளைவின் போக்கைக் கவனியுங்கள். அலாய் மற்ற கூறுகளின் தூய கூறுகளில் ஏதேனும் ஒன்றை நீங்கள் சேர்க்கும்போது, அதே தரத்தின் நேர்மறை அயனிகளின் கடுமையான ஏற்பாட்டில் சீரான தன்மை காணப்படுகிறது, இது லட்டு தளங்களில் தூய உலோகங்களில் காணப்படுகிறது. இதன் விளைவாக, ஒரு திடமான தீர்வு போன்ற ஒரு அலாய் ஒன்றில் எலக்ட்ரான்களை சிதறடிப்பது தூய்மையான கூறுகளின் படிக லட்டியின் சிதைவின் காரணமாக எந்தவொரு தூய கூறுகளையும் விட எப்போதும் அதிகமாக இருக்கும் அல்லது, அவர்கள் சொல்வது போல், படிக லட்டுகளின் குறைபாடு அதிகரிப்பதன் காரணமாக, அறிமுகப்படுத்தப்பட்ட ஒவ்வொரு அணுவும் தூய கூறுகளுடன் ஒப்பிடும்போது வேறுபட்ட வகையாகும் புள்ளி குறைபாடு. இதிலிருந்து திட தீர்வு வகையின் உலோகக் கலவைகளுக்கு, மேலும் ஒரு வகை எலக்ட்ரான் சிதறல் சேர்க்கப்படுகிறது - புள்ளி குறைபாடுகள் மற்றும் மின் எதிர்ப்பின் மூலம் சிதறல்.
T = 20 0 at இல் of இன் அனைத்து மதிப்புகளையும் மதிப்பிடுவது வழக்கம் என்பதால், திட தீர்வுகள் போன்ற உலோகக் கலவைகளை நிர்ணயிக்கும் காரணி புள்ளி குறைபாடுகளில் சிதறுகிறது. படிக லட்டியின் சரியான தன்மையின் மிகப்பெரிய மீறல்கள் ஐம்பது சதவிகிதம் செறிவுகளின் பகுதியில் காணப்படுகின்றன, வளைவு this இந்த பிராந்தியத்தில் அதிகபட்ச மதிப்பைக் கொண்டுள்ளது. உறவு 20 இலிருந்து TKS இன் எதிர்ப்பின் வெப்பநிலை குணகம் எதிர்ப்பு R க்கு நேர்மாறான விகிதாசாரத்தில் இருப்பதைக் காணலாம், எனவே குறிப்பிட்ட எதிர்ப்பு ρ; கூறுகளின் ஐம்பது சதவிகித விகிதத்தின் பிராந்தியத்தில் டி.கே.எஸ் வளைவு ஒரு நிமிடம் உள்ளது. ஆய்வகத்தின் இரண்டாம் பாகத்தில் உயர் குறிப்பிட்ட எதிர்ப்பைக் கொண்ட உலோகக் கலவைகள் கருதப்படுகின்றன. இத்தகைய பொருட்களில் உலோகக் கலவைகள் உள்ளன, அவை சாதாரண நிலைமைகளின் கீழ், குறைந்தபட்சம் 0.3 hOhm · m இன் குறிப்பிட்ட மின் எதிர்ப்பைக் கொண்டுள்ளன. இந்த பொருட்கள் பல்வேறு மின் அளவீட்டு மற்றும் மின்சார ஹீட்டர்கள், முன்மாதிரியான எதிர்ப்புகள், மின்தடையங்கள் போன்றவற்றின் உற்பத்தியில் பரவலாகப் பயன்படுத்தப்படுகின்றன. ஒரு விதியாக, உலோக அளவீட்டு கருவிகள், மாதிரி எதிர்ப்புகள் மற்றும் ரியோஸ்டாட்களை உற்பத்தி செய்ய உலோகக்கலவைகள் பயன்படுத்தப்படுகின்றன, அவை காலப்போக்கில் அவற்றின் குறிப்பிட்ட எதிர்ப்பின் உயர் நிலைத்தன்மை மற்றும் எதிர்ப்பின் குறைந்த வெப்பநிலை குணகம் ஆகியவற்றால் வேறுபடுகின்றன. இந்த பொருட்களில் மாங்கனின், கான்ஸ்டன்டான் மற்றும் நிக்ரோம் ஆகியவை அடங்கும். மங்கானின் ஒரு செப்பு-நிக்கல் அலாய் ஆகும், இது சராசரியாக 2.5 ... 3.5% நிக்கல் (கோபால்ட்டுடன்), 11.5 ... 13.5% மாங்கனீசு, 85.0 ... 89.0% செம்பு . மாங்கனீஸுடன் ஊக்கமளிப்பது, அதே போல் 400 ° C வெப்பநிலையில் ஒரு சிறப்பு வெப்ப சிகிச்சையை நடத்துதல், -100 முதல் + 100 ° C வரை வெப்பநிலை வரம்பில் மாங்கனின் எதிர்ப்பை உறுதிப்படுத்த அனுமதிக்கிறது. மங்கானின் ஒரு ஜோடியில் தெர்மோ-ஈ.எம்.எஃப் இன் மிகக் குறைந்த மதிப்பைக் கொண்டுள்ளது, இது காலத்தின் எதிர்ப்பின் உயர் நிலைத்தன்மையைக் கொண்டுள்ளது, இது மின்தடையங்கள் மற்றும் அதிக அளவீட்டு வகுப்புகளின் மின் அளவீட்டு கருவிகளின் உற்பத்தியில் பரவலாகப் பயன்படுத்த அனுமதிக்கிறது. கான்ஸ்டன்டனில் மாங்கனின் போன்ற கூறுகள் உள்ளன, ஆனால் வெவ்வேறு விகிதங்களில்: நிக்கல் (கோபால்ட்டுடன்) 39 ... 41%, மாங்கனீசு 1 ... 2%, தாமிர 56.1 ... 59.1%. அதன் மின் எதிர்ப்பு வெப்பநிலையைப் பொறுத்தது அல்ல. நிக்ரோம்கள் இரும்பு அடிப்படையிலான உலோகக் கலவைகள் ஆகும், அவை தரத்தைப் பொறுத்து, 15 ... 25% குரோமியம், 55 ... 78% நிக்கல், 1.5% மாங்கனீசு. இந்த உலோகக்கலவைகள் மற்றும் அவற்றின் ஆக்சைடு படங்களின் நேரியல் விரிவாக்கத்தின் வெப்பநிலை குணகங்களின் நெருங்கிய மதிப்புகள் காரணமாக அவை காற்றில் அதிக வெப்பநிலையில் நல்ல எதிர்ப்பைக் கொண்டிருப்பதால் அவை முக்கியமாக மின்சார வெப்பமூட்டும் கூறுகளின் உற்பத்திக்கு பயன்படுத்தப்படுகின்றன. பல்வேறு எதிர்ப்புக் கூறுகளின் உற்பத்திக்கு (நிக்ரோம் தவிர) பரவலாகப் பயன்படுத்தப்படும் உயர் எதிர்ப்பைக் கொண்ட உலோகக் கலவைகளில், வெப்ப-எதிர்ப்பு உலோகக் கலவைகள் ஃபெஹ்ரல் மற்றும் குரோம் ஆகியவற்றைக் கவனிக்க வேண்டியது அவசியம். அவை Fe-Cr-Al அமைப்பைச் சேர்ந்தவை, அவற்றின் கலவையில் 0.7% மாங்கனீசு, 0.6% நிக்கல், 12 ... 15% குரோமியம், 3.5 ... 5.5% அலுமினியம் மற்றும் மீதமுள்ள இரும்பு உள்ளது. இந்த உலோகக்கலவைகள் அதிக வெப்பநிலையில் பல்வேறு வாயு ஊடகங்களின் செல்வாக்கின் கீழ் மேற்பரப்பின் வேதியியல் அழிவுக்கு மிகவும் எதிர்ப்புத் தெரிவிக்கின்றன. 6.1 ஆய்வகப் பணிகளைச் செய்வதற்கான நடைமுறை எண் 2 அ நீங்கள் தொடங்குவதற்கு முன், படம் 11 இல் வழங்கப்பட்ட நிறுவல் வரைபடம் மற்றும் அளவீடுகளைச் செய்வதற்குத் தேவையான கருவிகளைப் பற்றி அறிந்து கொள்ளுங்கள். ஆய்வக அமைப்பானது ஒரு தெர்மோஸ்டாட்டைக் கொண்டுள்ளது, இதில் ஆய்வின் கீழ் உள்ள மாதிரிகள் அமைந்துள்ளன, மற்றும் ஒரு அளவிடும் பாலம் MO-62, இது ஒரு மாதிரியின் எதிர்ப்பை உண்மையான நேரத்தில் அளவிட உதவுகிறது. மாதிரிகள் கட்டாயமாக குளிரூட்டப்படுவதற்கு (T\u003e 25 ° C இல்) தெர்மோஸ்டாட்டில் ஒரு விசிறி நிறுவப்பட்டுள்ளது மற்றும் பின்புற மேற்பரப்பில் ஒரு தடுமாற்றம் உள்ளது. தெர்மோஸ்டாட்டின் வலது பக்கத்தில் மாதிரி எண் சுவிட்ச் உள்ளது.
படம் 11 - ஆய்வகப் பணிகளின் தோற்றம் மற்றும் அளவீட்டுத் திட்டம் 2 அ வேலையைத் தொடங்குவதற்கு முன், “N பெருக்கி” சுவிட்சுகளை 0.1 அல்லது 0.01 நிலைக்கு (அட்டவணையில் சுட்டிக்காட்டப்பட்டுள்ளபடி) அமைக்கவும், ஐந்து பத்து நாள் சுவிட்சுகள் - தீவிர இடது நிலைக்கு எதிரெதிர் திசையில் அமைத்து தெர்மோஸ்டாட் அணைக்கப்பட்டுள்ளதா என்பதை உறுதிப்படுத்தவும் (தெர்மோஸ்டாட்டின் முன் பேனலில் மாற்று சுவிட்ச் மேல் நிலையில் T≤25 ° C), இல்லையெனில், டம்பரைத் திறந்து, குறியீட்டு விளக்குக்கு கீழே அமைந்துள்ள மாற்று சுவிட்சைக் கொண்டு விசிறியை இயக்கவும், சாதாரண வெப்பநிலையை அடையும் வரை அதை கீழ் நிலைக்கு நகர்த்தவும், பின்னர் விசிறியை அணைக்கவும். 6.1.1. மாதிரி எண்ணை -1 ஆக அமைத்து, தெர்மோஸ்டாட்டில் நிறுவப்பட்ட ஒரு தெர்மோமீட்டரைப் பயன்படுத்தி அளவீடுகள் செய்யப்படும் வெப்பநிலையை சரிசெய்தல்; அளவிடும் பாலத்தின் பெருக்கத்தை 0.01 நிலைக்கு மாற்றவும், பின்னர் முன் பேனலின் மேல் வலதுபுறத்தில் அமைந்துள்ள மாற்று சுவிட்சைப் பயன்படுத்தி பிணையத்தை இயக்கவும், பிணைய காட்டி ஒளிரும். தசாப்த சுவிட்சுகளைப் பயன்படுத்தி, முதலில் அளவீட்டு பொத்தானை “சரியாக” அழுத்துவதன் மூலம் கால்வனோமீட்டர் ஊசி 0 இல் இருப்பதை உறுதிசெய்க. தொடர்ச்சியான தோராயங்களால் மிக உயர்ந்த தசாப்தத்தில் தொடங்குவதற்கான எதிர்ப்பைத் தேர்ந்தெடுப்பது, இதன் விளைவாக வரும் மதிப்பை காரணி மூலம் பெருக்கி அட்டவணை 3 இல் எழுதுங்கள். அடுத்த ஐந்து மாதிரிகளுக்கான அளவீடுகளை மீண்டும் செய்யவும், பின்னர் பெருக்கினை 0.1 நிலைக்கு மாற்றி 7-10 மாதிரிகளுக்கான அளவீடுகளைத் தொடரவும். 6.1.2 மாதிரி எண் சுவிட்சை அதன் அசல் நிலைக்குத் திருப்பி, தெர்மோஸ்டாட்டின் பின்புறத்தில் மடல் மூடி, தெர்மோஸ்டாட்டை இயக்கவும் (முன் பேனலில் உள்ள சுவிட்ச் முழுமையாக கீழே உள்ளது) மற்றும் மாதிரிகளை 50-70 ° C க்கு சூடாக்கி, பின்னர் தெர்மோஸ்டாட்டை அணைத்து, மடல் திறந்து உற்பத்தி செய்யுங்கள் 10 மாதிரிகளின் எதிர்ப்பின் அளவீட்டு பத்தி 6.1.1 ஐ ஒத்திருக்கிறது, ஒவ்வொரு அளவீட்டிற்கும் தொடர்புடைய வெப்பநிலையை பதிவு செய்கிறது. அட்டவணை 3 இல் பதிவுசெய்யப்பட்ட அனைத்து தரவுகளும் முடிவுகள் ஆசிரியரைக் காட்டுகின்றன. 6.2 வேலையைச் செய்வதற்கான நடைமுறை 2 பி நீங்கள் தொடங்குவதற்கு முன், படம் 12 இல் வழங்கப்பட்ட நிறுவல் வரைபடம் மற்றும் அதை செயல்படுத்த தேவையான கருவிகளைப் பற்றி அறிந்து கொள்ளுங்கள். நிறுவலில் ஒரு அளவீட்டு அலகு (பிஐ) உள்ளது, அங்கு + 12 வி மின்சாரம் அமைந்துள்ளது, வெப்பநிலை அளவீட்டு அலகு (பிஐடி), ஒரு தெர்மோஸ்டாட், அதில் மாதிரிகள் நிறுவப்பட்டுள்ளன, மாதிரிகள் கட்டாயமாக குளிரூட்டப்படுவதற்கான விசிறி, இயக்க முறைகள் மற்றும் வெப்பநிலையின் அறிகுறி, மாறுதல் வசதிகள் (மாதிரி எண்ணின் சுவிட்சுகள், இயக்க முறைமை, நெட்வொர்க்கில் மாறுதல், தெர்மோஸ்டாட் மற்றும் கட்டாய குளிர்ச்சியை இயக்குதல்), அத்துடன் ஒரு ஆர்.எல்.சி அலகு, பெறப்பட்ட பணிக்கு ஏற்ப அனைத்து மாதிரிகளின் எதிர்ப்பையும் உண்மையான நேரத்தில் அளவிட அனுமதிக்கிறது. .
படம் 12- ஆய்வகப் பணிகளின் தோற்றம் மற்றும் அளவீட்டுத் திட்டம் 2 பி நெட்வொர்க்கில் நிறுவலை மாற்றுவதற்கு முன், அளவிடும் அலகுக்கு வலது பக்கத்தில் அமைந்துள்ள கே 1 நெட்வொர்க்கின் சக்தி சுவிட்ச் மற்றும் ஆர்.எல்.சி மீட்டரின் சக்தி சுவிட்ச் ஆகியவை “ஆஃப்” நிலையில் இருப்பதை உறுதிசெய்க. 6.2.1 நெட்வொர்க் ஆர்.எல்.சி-மீட்டர் மற்றும் அளவீட்டு அலகு (பிஐ) இல் சேர்க்கவும். 6.2.2. சரியான நிலையில் BI இல் K2 மாற்று சுவிட்ச் (தெர்மோஸ்டாட் ஆஃப்), சிவப்பு எல்.ஈ. 6.2.3 BI செயல்பாட்டு முறை K4 மாற்று சுவிட்ச் கீழ் நிலையில் உள்ளது. 6.2.4 சுவிட்ச் "பெருக்கி" - 1: 100, 1: 1 (நடுத்தர நிலை) மாற்று. 6.2.5 பி 1 மற்றும் பி 2 (மாதிரி எண்கள்) - R1 நிலைக்கு மாறுகிறது. 6.2.6 கே 3 மாற்று சுவிட்ச் (விசிறி ஆன்) - முடக்கப்பட்டுள்ளது (கீழ் நிலை). 6.2.7 BI இன் மின்சக்தியை மாற்றவும் (BI இன் வலது பக்கத்தில் அமைந்துள்ள மாற்று சுவிட்ச் K1, “ஆன்” நிலையில் உள்ளது, பச்சை எல்.ஈ.டி விளக்குகள் உயர்ந்துள்ளன), மாற்று சுவிட்ச் “பெருக்கி” ஐ 1: 100 க்கு மாற்றவும், மாதிரிகளின் வெப்பநிலை 20 க்குள் இருப்பதை உறுதிப்படுத்தவும் 25. சி முன்னர் அலகு பின்புற பேனலில் ஒரு பொத்தானை அழுத்தி வெப்பநிலை காட்சியை இயக்கியுள்ளீர்கள், இல்லையெனில், தெர்மோஸ்டாட்டின் மூடியை BI மூடியிலுள்ள திருகு பயன்படுத்தி மேல்நோக்கி உயர்த்தி விசிறியை இயக்கவும், மாதிரிகளை குறிப்பிட்ட வரம்புகளுக்கு குளிர்விக்கவும். 6.2.8 ஆர்.எல்.சி-மீட்டரின் சக்தியை இயக்கி, அதன் மீது எதிர்ப்பு அளவீட்டு பயன்முறையைத் தேர்ந்தெடுக்கவும். 6.2.9 BI இல் உள்ள “N மாதிரி” சுவிட்சைப் பயன்படுத்தி, அறை வெப்பநிலையில் (20-25) 10 மாதிரிகளின் எதிர்ப்பை மாறி மாறி அளவிடவும், பின்னர் அதை அதன் அசல் நிலைக்குத் திருப்பி, அட்டவணை 3 இல் தரவை உள்ளிடவும். 6.2.10 BI இல் உள்ள தெர்மோஸ்டாட்டை இயக்கவும், நிலை K2 “ON” ஐ மாற்றவும் (சிவப்பு எல்.ஈ.டி விளக்குகள் வரை) மற்றும் 50-60 ° up வரை சூடாகவும், BI இல் விசிறி அட்டையை உயர்த்தி விசிறியை இயக்கவும் (K3 - up). 6.2.11 ஒவ்வொரு மாதிரிக்கும் அளவீட்டு செய்யப்பட்ட வெப்பநிலையை சரிசெய்யும்போது, பத்தி 6.2.9 ஐப் போலவே 10 மாதிரிகளின் எதிர்ப்பின் அளவீடுகளை செய்யுங்கள். தரவு அட்டவணை 3 இல் உள்ளிடப்பட வேண்டும். ஆரம்ப நிலையில் “N மாதிரி” ஐ மாற்றவும், பெருக்கி - நடுத்தர நிலையில் மாற்றவும். 6.2.12 தெர்மோஸ்டாட்டை T = 65 to க்கு வெப்பமாக்குவதைத் தொடரவும், விசிறி அட்டையை குறைக்கவும். தெர்மோஸ்டாட்டை அணைக்க, BI இல் உள்ள சுவிட்ச் K2 சரியான நிலையில் உள்ளது (சிவப்பு எல்.ஈ.டி முடக்கப்பட்டுள்ளது). 6.2.13 சுவிட்ச் கே 4 “ஆபரேஷன் பயன்முறையை” நிலை 2 க்கு பிஐ மற்றும் பெருக்கி 1: 1 நிலைக்கு மாற்றவும், விசிறி அட்டையை உயர்த்தவும். 6.2.14 ஒவ்வொரு (5-10) வெப்பநிலையிலும் (25-30) R1, R2, R3, R4 ஐ மாறி மாறி அளவிடவும் table மற்றும் அட்டவணையில் தரவை உள்ளிடவும் 4. வெப்பநிலை அடையும் போது (25-30) the பெருக்கி சுவிட்சை அமைக்கவும் - நடுத்தர நிலையில், பின்னர் இரு சாதனங்களிலும் பிணையத்தை அணைக்கவும். (மாதிரி 1-செம்பு, மாதிரி 2- நிக்கல், மாதிரி 3- மாறிலி, மாதிரி 4- நிக்ரோம்). அறிக்கையில் இருக்க வேண்டும்: வேலையின் நோக்கம்; நிறுவல் திட்டத்தின் சுருக்கமான விளக்கம்; வேலை செய்யும் சூத்திரங்கள், விளக்கங்கள், கணக்கீட்டின் எடுத்துக்காட்டுகள்; சோதனை முடிவுகள் அட்டவணை 1 (அல்லது அட்டவணைகள் 3 மற்றும் 4) மற்றும் Cu-Ag மற்றும் Cu-Ni அமைப்புகளுக்கான உலோகக் கலவைகளின் கலவையில் ρ மற்றும் TKS இன் சார்புகளின் இரண்டு வரைபடங்கள் மற்றும் 6.2.13-6.2.16 பிரிவுகளுக்கு - எதிர்ப்பின் சார்பு (R) t four நான்கு மாதிரிகளுக்கு; முடிவு முடிவுகள் சோதனை முடிவுகள் மற்றும் பரிந்துரைக்கப்பட்ட இலக்கியத்தின் ஆய்வு ஆகியவற்றை அடிப்படையாகக் கொண்டவை. அட்டவணை 3 - அலாய் கலவையில் ρ மற்றும் TKS இன் சார்பு பற்றிய ஆய்வு
கடத்தி நீளம் எல் = 2 மீ; பிரிவு S = 0.053 .m. அட்டவணை 4 வெப்பநிலையில் மாதிரி எதிர்ப்பின் சார்பு பற்றிய ஆய்வு
இலக்கியம் 1 பாசின்கோவ் வி.வி., சொரோகின் வி.எஸ். மின்னணு பொறியியல் பொருட்கள்: பாடநூல். - 2 வது பதிப்பு. - எம் .: அதிக. பள்ளி., 1986. - 367 பக். 2 மின் பொருட்களின் கையேடு / எட். ஒய் கோரிட்ஸ்கி, வி.வி. பாசின்கோவா, பி.எம். Tareeva. - எம் .: எனர்ஜோயிஸ்டாட், 1988. வி .3. கருவி மற்றும் ஆட்டோமேஷனில் உள்ள பொருட்கள். கையேடு / எட். YM: பியடினா, - எம் .: மாஷினோஸ்ட்ரோனி, 1982. 4 பொண்டரென்கோ ஜி.ஜி., கபனோவா டி.ஏ., ரைபல்கோ வி.வி. பொருட்கள் அறிவியல் .- எம் .: யுரேட் பப்ளிஷிங் ஹவுஸ், 2012. 359 ப. ρ · 10 2, டி.கே.எஸ் · 10 3, µohm · m 1 / ஆலங்கட்டி ஆக 100 80 60 40 20 0 கு 0 20 40 60 80 100 · · 10, டி.கே.எஸ், µohm · m 1 / ஆலங்கட்டி. Cu 100 80 60 40 20 0 நி 0 20 40 60 80 100 ஆசிரியருக்கான அட்டவணை - கிர்ஷினா I.A. - அசோக்., பி.எச்.டி. கிட்டத்தட்ட அனைத்து பொருட்களின் மின் எதிர்ப்பும் வெப்பநிலையைப் பொறுத்தது. இந்த சார்புடைய தன்மை வெவ்வேறு பொருட்களுக்கு வேறுபட்டது. ஒரு படிக அமைப்பைக் கொண்ட உலோகங்களில், எலக்ட்ரான்களை சார்ஜ் கேரியர்களாக இலவச பாதை படிக லட்டியின் தளங்களில் அமைந்துள்ள அயனிகளுடன் மோதினால் வரையறுக்கப்படுகிறது. மோதல்களில், எலக்ட்ரான்களின் இயக்க ஆற்றல் லட்டுக்கு மாற்றப்படுகிறது. ஒவ்வொரு மோதலுக்குப் பிறகு, எலக்ட்ரான்கள், மின்சார புல சக்திகளின் செயல்பாட்டின் கீழ், மீண்டும் வேகத்தை எடுக்கும், பின்வரும் மோதல்களின் போது வாங்கிய ஆற்றலை படிக லட்டுகளின் அயனிகளுக்கு அளிக்கிறது, அவற்றின் அதிர்வுகளை அதிகரிக்கிறது, இது பொருளின் வெப்பநிலையில் அதிகரிப்புக்கு வழிவகுக்கிறது. இதனால், மின் சக்தியை வெப்பமாக மாற்றுவதில் எலக்ட்ரான்களை இடைத்தரகர்களாகக் கருதலாம். வெப்பநிலையின் அதிகரிப்பு ஒரு பொருளின் துகள்களின் குழப்பமான வெப்ப இயக்கத்தின் அதிகரிப்புடன் சேர்ந்துள்ளது, இது அவற்றுடன் எலக்ட்ரான்களின் மோதல்களின் எண்ணிக்கையை அதிகரிக்க வழிவகுக்கிறது மற்றும் எலக்ட்ரான்களின் ஒழுங்கான இயக்கத்திற்கு இடையூறாக இருக்கிறது. பெரும்பாலான உலோகங்களுக்கு, இயக்க வெப்பநிலைக்குள், எதிர்ப்பானது நேர்கோட்டுடன் அதிகரிக்கிறது. எங்கே
T1i T2 - ஆரம்ப மற்றும் இறுதி வெப்பநிலை. இரண்டாவது வகையான கடத்திகளுக்கு, வெப்பநிலையின் அதிகரிப்பு அவற்றின் அயனியாக்கம் அதிகரிக்க வழிவகுக்கிறது; எனவே, இந்த வகை கடத்திகளின் டி.கே.எஸ் எதிர்மறையானது. பொருட்களின் எதிர்ப்பின் மதிப்புகள் மற்றும் அவற்றின் டி.கே.எஸ் ஆகியவை குறிப்பு புத்தகங்களில் கொடுக்கப்பட்டுள்ளன. வழக்கமாக, எதிர்ப்பின் மதிப்புகள் பொதுவாக +20 ° C வெப்பநிலையில் வழங்கப்படுகின்றன. கடத்தி எதிர்ப்பு வெளிப்பாட்டால் தீர்மானிக்கப்படுகிறது ஆர் 2 = ஆர் 1 பணி 3 எடுத்துக்காட்டுகம்பி குறுக்கு வெட்டு S = என்றால், செப்பு கம்பி இரண்டு கம்பி பரிமாற்றக் கோட்டின் எதிர்ப்பை + 20 ° C மற்றும் +40 ° C இல் தீர்மானிக்கவும். 120 மி.மீ. முடிவுகுறிப்பு அட்டவணைகளின்படி, எதிர்ப்பைக் காண்கிறோம்
R = சூத்திரத்தால் T1 = +20 ° C இல் கம்பியின் எதிர்ப்பை தீர்மானிக்கவும் ஆர் 1 = 0, 0175 + 40 ° C வெப்பநிலையில் கம்பிகளின் எதிர்ப்பு சூத்திரத்தால் நாம் காணலாம் (2.1.2) ஆர் 2 = 2.917 = 3.15 ஓம்ஸ். பணிநீளம் எல் கொண்ட காற்று மூன்று கம்பி வரி ஒரு கம்பி மூலம் செய்யப்படுகிறது, இதன் குறி அட்டவணை 2.1 இல் கொடுக்கப்பட்டுள்ளது. கொடுக்கப்பட்ட எடுத்துக்காட்டைப் பயன்படுத்தி “?” கையொப்பத்தால் குறிக்கப்பட்ட மதிப்பைக் கண்டுபிடிப்பது அவசியம் மற்றும் அட்டவணை 2.1 இல் குறிப்பிடப்பட்டுள்ள தரவுடன் விருப்பத்தைத் தேர்ந்தெடுக்கவும். சிக்கல், எடுத்துக்காட்டுக்கு மாறாக, ஒற்றை கம்பி கோடுடன் தொடர்புடைய கணக்கீடுகளை வழங்குகிறது என்பதை கவனத்தில் கொள்ள வேண்டும். இணைக்கப்படாத கம்பிகளின் தரங்களில், கடிதம் கம்பியின் பொருள் (ஏ - அலுமினியம்; எம் - செம்பு), மற்றும் எண் - இன் கம்பியின் குறுக்குவெட்டு ஆகியவற்றைக் குறிக்கிறதுமிமீ அட்டவணை 2.1
தலைப்பின் பொருள் பற்றிய ஆய்வு சோதனைகள் எண் 2 (TOE- ETM / PM "மற்றும் எண் 3 (TOE - ETM / IM) மின்னோட்டத்தை உருவாக்குவதில் ஈடுபடாத கடத்தி துகள்கள் (மூலக்கூறுகள், அணுக்கள், அயனிகள்) வெப்ப இயக்கத்தில் உள்ளன, மேலும் மின்னோட்டத்தை உருவாக்கும் துகள்கள் ஒரே நேரத்தில் வெப்பத்திலும், மின்சார புலத்தின் செயல்பாட்டின் கீழ் திசை இயக்கங்களிலும் உள்ளன. இதன் காரணமாக, மின்னோட்டத்தை உருவாக்கும் துகள்களுக்கும், அதன் உருவாக்கத்தில் ஈடுபடாத துகள்களுக்கும் இடையில், ஏராளமான மோதல்கள் உள்ளன, இதில் முதலாவது தற்போதைய மூல ஆற்றலின் ஒரு பகுதியை இரண்டாவதாக மாற்றும். மேலும் மோதல்கள், மின்னோட்டத்தை உருவாக்கும் துகள்களின் ஒழுங்கான இயக்கத்தின் வேகம் குறைகிறது. சூத்திரத்திலிருந்து காணலாம் I = enνS, வேகம் குறைவது மின்னோட்டத்தின் குறைவுக்கு வழிவகுக்கிறது. ஆம்பரேஜைக் குறைக்க நடத்துனரின் சொத்தை வகைப்படுத்தும் அளவிடல் அளவு அழைக்கப்படுகிறது கடத்தி எதிர்ப்பு. ஓம் சட்டத்தின் சூத்திரத்திலிருந்து, எதிர்ப்பு கடத்தியின் எதிர்ப்பு அதன் நீளம் எல், குறுக்கு வெட்டு எஸ் மற்றும் பொருள் ஆகியவற்றைப் பொறுத்தது, இது எதிர்ப்பால் வகைப்படுத்தப்படுகிறது மின்சார புலத்தின் செயல்பாட்டின் கீழ், மோதல்களுக்கு இடையில் ஒரு மின்னோட்டத்தை உருவாக்கும் துகள்கள் வேகமாக நகர்கின்றன, புலம் ஆற்றல் காரணமாக அவற்றின் இயக்க ஆற்றலை அதிகரிக்கும். மின்னோட்டத்தை உருவாக்காத துகள்களுடன் மோதுகையில், அவை அவற்றின் இயக்க ஆற்றலின் ஒரு பகுதியை அவர்களுக்கு மாற்றும். இதன் விளைவாக, கடத்தியின் உள் ஆற்றல் அதிகரிக்கிறது, இது வெளிப்புறமாக அதன் வெப்பத்தில் வெளிப்படுகிறது. வெப்பமடையும் போது கடத்தியின் எதிர்ப்பு மாறுகிறதா என்பதைக் கவனியுங்கள்.
மின்சுற்றில் எஃகு கம்பியின் சுருள் உள்ளது (சரம், படம் 81, அ). சுற்று மூடப்பட்ட பிறகு, நாங்கள் கம்பி வெப்பப்படுத்த ஆரம்பிக்கிறோம். நாம் அதை எவ்வளவு சூடாக்குகிறோமோ, அவ்வளவு குறைவான ஆம்பரேஜ் காட்டுகிறது. உலோகங்கள் சூடாகும்போது, அவற்றின் எதிர்ப்பு அதிகரிக்கும் என்பதே இதன் குறைவு. எனவே, ஒரு ஒளி விளக்கை முடி அணைக்கும்போது அதன் எதிர்ப்பு தோராயமாக இருக்கும் 20 ஓம்அதை எரியும் போது (2900 ° C) - 260 ஓம். ஒரு உலோகம் வெப்பமடையும் போது, எலக்ட்ரான்களின் வெப்ப இயக்கம் மற்றும் படிக லட்டுகளில் அயனிகளின் அலைவு விகிதம் அதிகரிக்கிறது, இதன் விளைவாக அயனிகளுடன் மின்னோட்டத்தை உருவாக்கும் எலக்ட்ரான்களின் மோதல்களின் எண்ணிக்கை அதிகரிக்கிறது. இது கடத்தி எதிர்ப்பின் அதிகரிப்புக்கு காரணமாகிறது *. உலோகங்களில், இலவசமற்ற எலக்ட்ரான்கள் அயனிகளுடன் மிகவும் வலுவாக பிணைக்கப்பட்டுள்ளன; எனவே, உலோகங்கள் சூடாகும்போது, இலவச எலக்ட்ரான்களின் எண்ணிக்கை கிட்டத்தட்ட மாறாமல் இருக்கும். * (மின்னணு கோட்பாட்டின் அடிப்படையில், வெப்பநிலையின் எதிர்ப்பை சார்ந்து இருப்பதற்கான சரியான சட்டத்தை பெற முடியாது. அத்தகைய சட்டம் குவாண்டம் கோட்பாட்டின் மூலம் நிறுவப்பட்டுள்ளது, இதில் ஒரு எலக்ட்ரான் அலை பண்புகளைக் கொண்ட ஒரு துகள் என்று கருதப்படுகிறது, மேலும் எலக்ட்ரான் அலைகளை பரப்புவதற்கான ஒரு செயல்முறையாக ஒரு உலோகத்தின் வழியாக ஒரு கடத்தல் எலக்ட்ரானின் இயக்கம், அதன் நீளம் டி ப்ரோக்லி உறவால் தீர்மானிக்கப்படுகிறது.) வெவ்வேறு பொருட்களின் கடத்திகளின் வெப்பநிலை ஒரே எண்ணிக்கையிலான டிகிரிகளால் மாறும்போது, அவற்றின் எதிர்ப்பு சமமாக மாறுபடும் என்பதை சோதனைகள் காட்டுகின்றன. உதாரணமாக, செப்பு கடத்திக்கு எதிர்ப்பு இருந்தால் 1 ஓம்பின்னர் சூடாக்கப்பட்ட பிறகு 1. C. அவருக்கு எதிர்ப்பு இருக்கும் 1,004 ஓம்மற்றும் டங்ஸ்டன் - 1,005 ஓம் ஒரு கடத்தியின் எதிர்ப்பை அதன் வெப்பநிலையில் சார்ந்து இருப்பதைக் குறிக்க, ஒரு அளவு அறிமுகப்படுத்தப்படுகிறது, இது எதிர்ப்பின் வெப்பநிலை குணகம் என்று அழைக்கப்படுகிறது. 1 ஓமில் ஒரு கடத்தியின் எதிர்ப்பின் மாற்றத்தால் அளவிடப்படும் ஒரு அளவிடுதல் அளவு, 0 ° C இல் எடுக்கப்படுகிறது, அதன் வெப்பநிலையில் 1 ° C மாற்றத்தால், எதிர்ப்பின் வெப்பநிலை குணகம் called. எனவே, டங்ஸ்டனுக்கு, இந்த குணகம் சமம் 0.005 டிகிரி -1தாமிரத்திற்கு - 0.004 டிகிரி -1. எதிர்ப்பின் வெப்பநிலை குணகம் வெப்பநிலையைப் பொறுத்தது. உலோகங்களைப் பொறுத்தவரை, இது வெப்பநிலையுடன் சிறிது மாறுபடும். ஒரு சிறிய வெப்பநிலை வரம்பில், இந்த பொருளுக்கு இது நிலையானதாகக் கருதப்படுகிறது. கடத்தியின் எதிர்ப்பைக் கணக்கிடும் ஒரு சூத்திரத்தை நாங்கள் பெறுகிறோம், அதன் வெப்பநிலையை கணக்கில் எடுத்துக்கொள்கிறோம். என்று கருதுங்கள் ஆர் 0 - கடத்தி எதிர்ப்பு 0. C.சூடாகும்போது 1. C. அது அதிகரிக்கும் αR 0, மற்றும் சூடாகும்போது t ° - ஆன் αRt ° மற்றும் ஆகிறது R = R 0 + αR 0 t °அல்லது வெப்பநிலையில் உலோகங்களின் எதிர்ப்பின் சார்பு கணக்கில் எடுத்துக்கொள்ளப்படுகிறது, எடுத்துக்காட்டாக, மின்சார ஹீட்டர்கள், விளக்குகள் ஆகியவற்றிற்கான சுருள்களை தயாரிப்பதில்: சுழல் கம்பியின் நீளம் மற்றும் அனுமதிக்கக்கூடிய ஆம்பரேஜ் ஆகியவை சூடான நிலையில் அவற்றின் எதிர்ப்பிலிருந்து கணக்கிடப்படுகின்றன. வெப்பநிலையின் மீதான உலோகங்களின் எதிர்ப்பின் சார்பு எதிர்ப்பு வெப்பமானிகளில் பயன்படுத்தப்படுகிறது, அவை வெப்ப இயந்திரங்கள், எரிவாயு விசையாழிகள், குண்டு வெடிப்பு உலைகளில் உலோகம் போன்றவற்றின் வெப்பநிலையை அளவிடப் பயன்படுகின்றன. இந்த வெப்பமானி பீங்கானால் செய்யப்பட்ட ஒரு சட்டகத்தின் மீது மெல்லிய பிளாட்டினம் (நிக்கல், இரும்பு) சுருள் காயத்தைக் கொண்டுள்ளது. ஒரு பாதுகாப்பு வழக்கில். அதன் முனைகள் ஒரு மின்சுற்றில் ஒரு அம்மீட்டருடன் சேர்க்கப்பட்டுள்ளன, இதன் அளவு டிகிரிகளில் பட்டம் பெற்றது. ஹெலிக்ஸ் வெப்பமடையும் போது, சுற்றில் உள்ள மின்னோட்டம் குறைகிறது, இதனால் அம்மீட்டர் ஊசி நகரும், இது வெப்பநிலையைக் காட்டுகிறது. இந்த பகுதியின் எதிர்ப்பின் தலைகீழ், சங்கிலி என்று அழைக்கப்படுகிறது மின் கடத்தல் கடத்தி (மின் கடத்துத்திறன்). கடத்தியின் கடத்துத்திறன் கடத்தியின் அதிக கடத்துத்திறன், அதன் எதிர்ப்பைக் குறைத்து, மின்னோட்டத்தை சிறப்பாக நடத்துகிறது. கடத்துத்திறன் அலகு பெயர் உலோகங்களின் வெப்பநிலை எதிர்ப்பு குறைகிறது. ஆனால் உலோகங்கள் மற்றும் உலோகக் கலவைகள் உள்ளன, அவற்றின் எதிர்ப்பானது ஒவ்வொரு உலோகத்திற்கும் அலாய்க்கும் நிர்ணயிக்கப்பட்ட குறைந்த தாவலில், திடீரென குறைந்து மறைந்து சிறியதாகிவிடும் - கிட்டத்தட்ட பூஜ்ஜியம் (அத்தி. 81, பி). வருகிறது மீக்கடத்தல் - நடத்துனருக்கு நடைமுறையில் எந்த எதிர்ப்பும் இல்லை, ஒரு முறை நடத்துனர் சூப்பர் கண்டக்டிவிட்டி வெப்பநிலையில் இருக்கும்போது அதில் உற்சாகமாக இருக்கும் மின்னோட்டம் நீண்ட காலமாக உள்ளது (ஒரு சோதனையில் மின்னோட்டம் ஒரு வருடத்திற்கும் மேலாக காணப்பட்டது). ஒரு மின்னோட்டத்தை சூப்பர் கண்டக்டர் வழியாக அனுப்பும்போது 1200 அ / மிமீ 2 வெப்ப வெளியீடு எதுவும் காணப்படவில்லை. மின்னோட்டத்தின் சிறந்த கடத்திகளான மோனோவெலண்ட் உலோகங்கள், சோதனைகள் மேற்கொள்ளப்பட்ட மிகக் குறைந்த வெப்பநிலை வரை சூப்பர் கண்டக்டிங் நிலைக்குச் செல்லாது. உதாரணமாக, இந்த சோதனைகளில், தாமிரம் குளிரூட்டப்பட்டது 0,0156 ° K, தங்கம் - க்கு 0.0204 ° கே. சாதாரண வெப்பநிலையில் சூப்பர் கண்டக்டிவிட்டி கொண்ட உலோகக்கலவைகளைப் பெற முடிந்தால், இது மின் பொறியியலுக்கு மிகவும் முக்கியத்துவம் வாய்ந்ததாக இருக்கும். நவீன கருத்துகளின்படி, சூப்பர் கண்டக்டிவிட்டிக்கு முக்கிய காரணம் பிணைக்கப்பட்ட எலக்ட்ரான் ஜோடிகளின் உருவாக்கம் ஆகும். இலவச எலக்ட்ரான்களுக்கு இடையிலான சூப்பர் கண்டக்டிவிட்டி வெப்பநிலையில், பரிமாற்ற சக்திகள் செயல்படத் தொடங்குகின்றன, இதனால் எலக்ட்ரான்கள் பிணைக்கப்பட்ட எலக்ட்ரான் ஜோடிகளை உருவாக்குகின்றன. பிணைக்கப்பட்ட எலக்ட்ரான் ஜோடிகளிலிருந்து அத்தகைய எலக்ட்ரான் வாயு சாதாரண எலக்ட்ரான் வாயுவை விட வேறுபட்ட பண்புகளைக் கொண்டுள்ளது - இது ஒரு சூப்பர் கண்டக்டரில் லட்டு தளங்களைப் பற்றிய உராய்வு இல்லாமல் நகர்கிறது. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
மிகவும் பிரபலமான:
புதிய
- திறந்த பாடம் "திருத்துதல், வளைத்தல்"
- படிக்கட்டுகள் மற்றும் தளங்களை நிறுவுதல்: பொது தகவல்
- குடியிருப்பில் நீர் வழங்கல் குழாய்களை சரிசெய்தல் எஃகு குழாய்களை சரிசெய்தல்
- மார்க்அப் வரையறை. பிளானர் குறித்தல். மார்க்அப் வகைகள். சுய சோதனைக்கான கேள்விகள்
- குழாய் வளைக்கும் இயந்திரங்கள் குழாய் வளைக்கும் இயந்திரத்தின் பல்வேறு வேறுபாடுகள்
- தாக்கல் செய்யும் போது பாதுகாப்பு
- ஸ்கிரிபரின் கூர்மையான கோணம் என்னவாக இருக்க வேண்டும்
- எதிர்கால உற்பத்தியின் வரையறைகளை தயாரிப்பதில் வரைதல்
- உலோகத்தை வெட்டுவதற்கான நவீன வழிகள் மற்றும் அதன் குறைபாடுகள்
- கெர்னர் - அதனால் துரப்பணம் நழுவாது!

 ,
(9)
,
(9)
 (10)
(10)

 (11)
(11) (13)
(13) ,
(14)
,
(14)
 ,
(15)
,
(15)

 (17)
(17) (18)
(18) ,
, ,
,


 l மற்றும் குறுக்கு வெட்டு எஸ்
l மற்றும் குறுக்கு வெட்டு எஸ்  அறியப்பட்ட போதைப்பொருளால் வெளிப்படுத்தப்படுகிறது
அறியப்பட்ட போதைப்பொருளால் வெளிப்படுத்தப்படுகிறது (19)
(19)
 (20)
(20) (21)
(21)

 ;
;
 .
. மற்றும்
மற்றும்  - ஆரம்ப மற்றும் இறுதி வெப்பநிலையில் குறிப்பிட்ட எதிர்ப்புகள்;
- ஆரம்ப மற்றும் இறுதி வெப்பநிலையில் குறிப்பிட்ட எதிர்ப்புகள்; - இந்த உலோக குணகத்திற்கான நிலையானது, எதிர்ப்பின் வெப்பநிலை குணகம் (டி.கே.எஸ்) என அழைக்கப்படுகிறது;
- இந்த உலோக குணகத்திற்கான நிலையானது, எதிர்ப்பின் வெப்பநிலை குணகம் (டி.கே.எஸ்) என அழைக்கப்படுகிறது; (2.1.2)
(2.1.2) மற்றும் கோட்டின் நீளம் l = 10 கி.மீ.
மற்றும் கோட்டின் நீளம் l = 10 கி.மீ. + 20 ° C இல் தாமிரம் மற்றும் எதிர்ப்பின் வெப்பநிலை குணகம்
+ 20 ° C இல் தாமிரம் மற்றும் எதிர்ப்பின் வெப்பநிலை குணகம்  :
: = 0,0175 ஓம் மி.மீ.
= 0,0175 ஓம் மி.மீ.  / மீ;
/ மீ;  = 0.004 டிகிரி
= 0.004 டிகிரி  .
. , கோட்டின் முன்னோக்கி மற்றும் தலைகீழ் கம்பிகளின் நீளம் கொடுக்கப்பட்டால்:
, கோட்டின் முன்னோக்கி மற்றும் தலைகீழ் கம்பிகளின் நீளம் கொடுக்கப்பட்டால்: 2 = 2.917 ஓம்ஸ்.
2 = 2.917 ஓம்ஸ். .
.