|
Ir arī ierobežojumi atomu kodolu pastāvēšanai no supersmagajiem elementiem. Dabiskos apstākļos elementi ar Z > 92 nav atrasti. Aprēķini, izmantojot šķidruma pilienu modeli, paredz šķelšanās barjeras izzušanu kodoliem, kuru Z2/A ≈ 46 (aptuveni 112. elements). Supersmago kodolu sintēzes problēmā jāizšķir divas problēmu jomas.
- Kādām īpašībām vajadzētu būt īpaši smagajiem kodoliem? Vai šajā apgabalā Z un N būs maģiski skaitļi. Kādi ir supersmago kodolu galvenie sabrukšanas kanāli un pussabrukšanas periodi?
- Kādas reakcijas jāizmanto, lai sintezētu supersmagos kodolus, bombardējošo kodolu veidus, paredzamās šķērsgriezuma vērtības, saliktā kodola paredzamās ierosmes enerģijas un deeksitācijas kanālus?
Tā kā supersmago kodolu veidošanās notiek mērķa kodola un krītošās daļiņas pilnīgas saplūšanas rezultātā, ir nepieciešams izveidot teorētiskus modeļus, kas apraksta divu sadursmju kodolu saplūšanas procesa dinamiku saliktā kodolā.
Supersmago elementu sintezēšanas problēma ir cieši saistīta ar faktu, ka kodoliem ar Z,N = 8, 20, 28, 50, 82, N = 126 (maģiski skaitļi) ir paaugstināta stabilitāte attiecībā uz dažādiem radioaktīvās sabrukšanas veidiem. Šī parādība ir izskaidrota čaulas modeļa ietvaros - burvju skaitļi atbilst aizpildītiem apvalkiem. Protams, rodas jautājums par šādu maģisko skaitļu esamību Z un N. Ja tie eksistē atomu kodolu N-Z diagrammas apgabalā N > 150, Z > 101, ir jānovēro supersmagie kodoli ar palielinātiem pussabrukšanas periodiem, t.i. ir jābūt stabilitātes salai. Darbā, balstoties uz aprēķiniem, kas veikti, izmantojot Vudsa-Saksona potenciālu, ņemot vērā spin-orbītas mijiedarbību, tika parādīts, ka kodolu stabilitātes pieaugums ir sagaidāms kodolam ar Z = 114, tas ir, nākamais piepildīts protonu apvalks atbilst Z = 114, piepildītais neitronu apvalks atbilst skaitlim N ~
184. Slēgtas čaulas var būtiski palielināt skaldīšanas barjeras augstumu un attiecīgi palielināt kodola kalpošanas laiku. Tādējādi šajā kodolu reģionā (Z = 114, N ~
184) jums vajadzētu meklēt Stabilitātes salu. Tas pats rezultāts tika iegūts patstāvīgi darbā.
Kodoli ar Z = 101–109 tika atklāti pirms 1986. gada un tika nosaukti: 101 - Md (Menelevium), 102 - No (Nobelium), 103 - Lr (Lawrencium), 104 - Rf (Rutherfordium, 106 - Sg (Seaborgium), 107 - Ns (Nielsborium), 108 - Hs (Hassium), 109 - Mt (Meitnerium), ņemot vērā Dubnas pētnieku nopelnus liela skaita smago elementu izotopu (102-105) atklāšanā, 1997.g. ar Tīras un lietišķās ķīmijas Ģenerālās asamblejas lēmumu elementam ar Z = 105 tika piešķirts nosaukums Dubnium (Db) Šo elementu iepriekš sauca par Ha (Hannium).

Rīsi. 12.3. Izotopu Ds (Z = 110), Rg (Z = 111), Cn (Z = 112) sabrukšanas ķēdes.
Jauns posms supersmago kodolu izpētē sākās 1994. gadā, kad tika ievērojami palielināta reģistrācijas efektivitāte un uzlabota supersmago kodolu novērošanas tehnika. Rezultātā tika atklāti izotopi Ds (Z = 110), Rg (Z = 111) un Cn (Z = 112).
Lai iegūtu supersmagos kodolus, tika izmantoti paātrināti 50 Ti, 51 V, 58 Fe, 62 Ni, 64 Ni, 70 Zn un 82 Se stari. Kā mērķi tika izmantoti izotopi 208 Pb un 209 Bi. Nosauktajā Kodolreakciju laboratorijā tika sintezēti dažādi elementa 110 izotopi. G.N. Flerovs, izmantojot reakciju 244 Pu(34 S,5n) 272 110 un GSI (Darmstadt) reakcijā 208 Pb(62 Ni,n) 269 110. Izotopi 269 Ds, 271 Ds, 272 Rg un 277 Cn tika reģistrēti atbilstoši uz to sabrukšanas ķēdēm (12.3. att.).
Liela loma supersmago elementu ražošanā ir teorētiskajiem modeļiem, ar kuru palīdzību tiek aprēķinātas ķīmisko elementu paredzamās īpašības un reakcijas, kurās tie var veidoties.
Pamatojoties uz dažādiem teorētiskiem modeļiem, tika aprēķināti supersmago kodolu sabrukšanas raksturlielumi. Viena šāda aprēķina rezultāti ir parādīti attēlā. 12.4. Pat supersmago kodolu pussabrukšanas periodi ir norādīti attiecībā uz spontānu skaldīšanu (a), α-sabrukšanu (b), β-sabrukšanu (c) un visiem iespējamiem sabrukšanas procesiem (d). Visstabilākais kodols attiecībā uz spontānu skaldīšanu (12.4.a att.) ir kodols ar Z = 114 un N = 184. Tam pussabrukšanas periods attiecībā uz spontānu skaldīšanu ir ~10 16 gadi. Elementa 114 izotopiem, kas no stabilākā atšķiras par 6-8 neitroniem, pussabrukšanas periodi samazinās par
10-15 kārtas. Pussabrukšanas periodi attiecībā pret α-sabrukšanu ir parādīti attēlā. 12.5b. Visstabilākais kodols atrodas reģionā Z = 114 un N = 184 (T 1/2 = 10 15 gadi).
Kodoli, kas ir stabili attiecībā uz β-sabrukšanu, ir parādīti attēlā. 12.4v ar tumšiem punktiem. Attēlā Attēlā 12.4d parādīti kopējie pussabrukšanas periodi, kas pāra-pāra kodoliem, kas atrodas centrālās kontūras iekšpusē, ir ~10 5 gadi. Tādējādi, ņemot vērā visus sabrukšanas veidus, izrādās, ka kodoli Z = 110 un N = 184 tuvumā veido "stabilitātes salu". 294 110 kodola pussabrukšanas periods ir aptuveni 10 9 gadi. Atšķirība starp Z vērtību un burvju skaitli 114, ko paredz čaulas modelis, ir saistīta ar konkurenci starp skaldīšanu (attiecībā pret kuru kodols ar Z = 114 ir visstabilākais) un α-sabrukšanu (attiecībā pret kuriem kodoli ar zemāku Z ir stabils). Nepāra pāra un pāra pāra kodoliem ir pusperiods attiecībā pret
α-sabrukšana un spontāna skaldīšanās palielinās, un attiecībā pret β-sabrukšanu tie samazinās. Jāatzīmē, ka iepriekš minētie aprēķini ir ļoti atkarīgi no aprēķinos izmantotajiem parametriem, un tos var uzskatīt tikai par norādi uz iespējamību, ka pastāv supersmagi kodoli, kuru kalpošanas laiks ir pietiekami ilgs to eksperimentālai noteikšanai.

Rīsi. 12.4. Pussabrukšanas periodi, kas aprēķināti pāra vai pat supersmagiem kodoliem (skaitļi norāda pussabrukšanas periodus gados):
a - attiecībā uz spontānu skaldīšanu, b - α-sabrukšanu, c - e-tveršanu un β-sabrukšanu, d - visiem sabrukšanas procesiem
Cita supersmago kodolu līdzsvara formas un to pussabrukšanas perioda aprēķina rezultāti ir parādīti attēlā. 12.5., 12.6. Attēlā 12.5. attēlā parādīta līdzsvara deformācijas enerģijas atkarība no neitronu un protonu skaita kodoliem ar Z = 104-120. Deformācijas enerģiju definē kā starpību starp kodolu enerģijām līdzsvarā un sfēriskā formā. No šiem datiem ir skaidrs, ka apgabalā Z = 114 un N = 184 ir jābūt kodoliem, kuriem pamatstāvoklī ir sfēriska forma. Visi līdz šim atklātie supersmagie kodoli (tie parādīti 12.5. attēlā kā tumši dimanti) ir deformēti. Vieglie dimanti parāda kodolus, kas ir stabili attiecībā pret β-sabrukšanu. Šiem kodoliem jāsadalās ar α sabrukšanu vai skaldīšanu. Galvenajam sabrukšanas kanālam jābūt α-sabrukumam.
Pussabrukšanas periodi vienmērīgiem β-stabiliem izotopiem ir parādīti attēlā. 12.6. Saskaņā ar šīm prognozēm lielākajai daļai kodolu ir sagaidāms daudz ilgāks pussabrukšanas periods nekā jau atklātajiem supersmagajiem kodoliem (0,1–1 ms). Piemēram, 292 Ds kodolam tiek prognozēts ~ 51 gads.
Tādējādi saskaņā ar mūsdienu mikroskopiskiem aprēķiniem supersmago kodolu stabilitāte strauji palielinās, kad tie tuvojas neitronu maģiskajam skaitlim N = 184. Vēl nesen vienīgais elementa Z = 112 Cn (kopernicijs) izotops bija izotops 277 Cn, kuram ir pussabrukšanas periods ir 0,24 ms. Smagākais izotops 283 Cn tika sintezēts aukstās saplūšanas reakcijā 48 Ca + 238 U. Apstarošanas laiks bija 25 dienas. Kopējais 48 Ca jonu skaits uz mērķa ir 3,5 · 10 18. Tika reģistrēti divi gadījumi, kas tika interpretēti kā iegūtā izotopa 283 Cn spontāna skaldīšanās. Paredzamais šī jaunā izotopa pussabrukšanas periods ir T 1/2 = 81 s. Tādējādi ir skaidrs, ka neitronu skaita palielināšanās 283 Cn izotopu salīdzinājumā ar 277 Cn izotopu par 6 vienībām palielina kalpošanas laiku par 5 kārtībām.
Attēlā 12.7., kas ņemts no darba, eksperimentāli izmērītie α-sabrukšanas periodi tiek salīdzināti ar teorētisko aprēķinu rezultātiem, pamatojoties uz šķidruma pilienu modeli, neņemot vērā kodolu čaulas struktūru. Var redzēt, ka visiem smagajiem kodoliem, izņemot vieglos urāna izotopus, čaulas ietekme palielina pussabrukšanas periodu par 2–5 kārtībām lielākajai daļai kodolu. Kodola apvalka struktūrai ir vēl spēcīgāka ietekme uz relatīvi spontānas skaldīšanas pussabrukšanas periodu. Pu izotopu pussabrukšanas perioda pieaugums ir vairākas kārtas un palielinās 260 Sg izotopam.
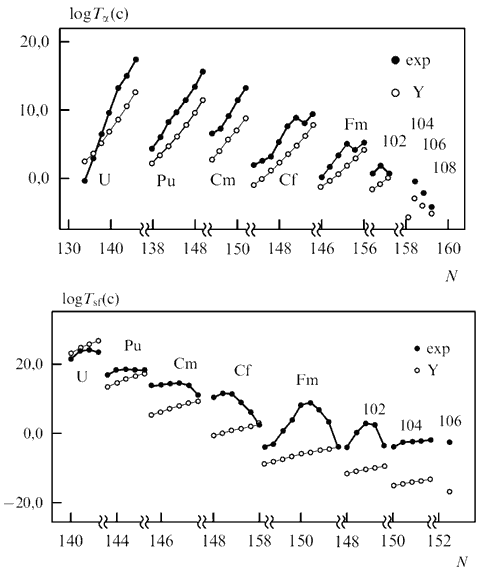
Rīsi. 12.7. Eksperimentāli izmērīti (● exp) un teorētiski aprēķināti (○ Y) transurāna elementu pussabrukšanas periodi, pamatojoties uz šķidruma pilienu modeli, neņemot vērā kodola apvalka struktūru. Augšējā attēlā ir α-sabrukšanas pussabrukšanas periods, bet apakšējā attēlā ir spontānas skaldīšanas pussabrukšanas periods. Attēlā 12.8. attēlā parādīts mērītais seaborgija izotopu Sg (Z = 106) mūža ilgums salīdzinājumā ar dažādu teorētisko modeļu prognozēm. Ievērības cienīgs ir izotopa mūža samazinājums ar N = 164 gandrīz par lielumu, salīdzinot ar izotopa mūža ilgumu ar N = 162.
Vistuvāko pieeju stabilitātes salai var panākt reakcijā 76 Ge + 208 Pb. Sapludināšanas reakcijā var izveidoties supersmags, gandrīz sfērisks kodols, kam seko γ kvantu vai viena neitrona emisija. Saskaņā ar aplēsēm iegūtajam 284 114 kodolam vajadzētu sabrukt, izdalot α daļiņas ar pussabrukšanas periodu ~ 1 ms. Papildu informāciju par čaulas noslogojumu reģionā N = 162 var iegūt, pētot 271 Hs un 267 Sg kodolu α sabrukšanu. Šiem kodoliem tiek prognozēts 1 minūtes pussabrukšanas periods. un 1 stundu. Kodoliem 263 Sg, 262 Bh, 205 Hs, 271 273 Ds sagaidāma izomērijas izpausme, kuras iemesls ir apakščaulu piepildīšanās ar j = 1/2 un j = 13/2 reģionā N = 162 kodoliem. deformēts pamatstāvoklī.
Attēlā 12.9. attēlā parādītas eksperimentāli izmērītās ierosmes funkcijas elementu Rf (Z = 104) un Hs (Z = 108) veidošanās reakcijai krītošo jonu 50 Ti un 56 Fe saplūšanas reakcijām ar mērķa kodolu 208 Pb.
Iegūtais savienojuma kodols tiek atdzesēts, izlaižot vienu vai divus neitronus. Informācija par smago jonu saplūšanas reakciju ierosmes funkcijām ir īpaši svarīga supersmago kodolu iegūšanai. Smago jonu saplūšanas reakcijā ir nepieciešams precīzi līdzsvarot Kulona spēku un virsmas spraiguma spēku ietekmi. Ja krītošā jona enerģija nav pietiekami liela, tad binārās kodolsistēmas saplūšanai ar minimālo pietuvošanās attālumu nepietiks. Ja krītošās daļiņas enerģija ir pārāk augsta, tad iegūtajai sistēmai būs augsta ierosmes enerģija un tā, visticamāk, sadalīsies fragmentos. Efektīva saplūšana notiek diezgan šaurā sadursmju daļiņu enerģijas diapazonā.

12.10.att. 64 Ni un 208 Pb saplūšanas potenciālu diagramma.
Kodolsintēzes reakcijas ar minimālu neitronu skaitu (1–2) ir īpaši interesantas, jo sintezētajos supersmagajos kodolos vēlams pēc iespējas lielāku N/Z attiecību. Attēlā 12.10. attēlā parādīts kodolu saplūšanas potenciāls reakcijā 64 Ni + 208 Pb → 272 Ds. Vienkāršākie aprēķini liecina, ka tuneļa efekta iespējamība kodolsintēzes gadījumā ir ~10–21, kas ir ievērojami mazāka par novēroto šķērsgriezuma vērtību. To var izskaidrot šādi. 14 fm attālumā starp kodolu centriem sākotnējo kinētisko enerģiju 236, 2 MeV pilnībā kompensē Kulona potenciāls. Šajā attālumā saskaras tikai nukleoni, kas atrodas uz kodola virsmas. Šo nukleonu enerģija ir zema. Tāpēc pastāv liela varbūtība, ka nukleoni vai nukleonu pāri atstās orbitāles vienā kodolā un pārvietosies uz partnera kodola brīvajiem stāvokļiem. Nukleonu pārnešana no krītoša kodola uz mērķa kodolu ir īpaši pievilcīga gadījumā, ja par mērķi tiek izmantots divkārši maģiskais svina izotops 208 Pb. 208 Pb ir aizpildīts protonu apakščaulas h 11/2 un neitronu apakščaulas h 9/2 un i 13/2. Sākotnēji protonu pārnesi stimulē protonu-protonu pievilcības spēki, bet pēc h 9/2 apakščaulas aizpildīšanas - protonu-neitronu pievilcības spēki. Līdzīgi neitroni pārvietojas brīvajā apakščaulā i 11/2, ko piesaista neitroni no jau piepildītā apakščaula i 13/2. Savienošanas enerģijas un lielo orbitālo leņķisko momentu dēļ nukleonu pāra pārnešana ir lielāka iespējamība nekā viena nukleona pārnešana. Pēc divu protonu pārnešanas no 64 Ni 208 Pb Kulona barjera samazinās par 14 MeV, kas veicina mijiedarbojošo jonu ciešāku kontaktu un nukleonu pārneses procesa turpināšanu.
Darbos [V.V. Volkovs. Dziļu neelastīgu pārnesumu kodolreakcijas. M. Energoizdats, 1982; V.V. Volkovs. Izv. PSRS Zinātņu akadēmija, fiziskā sērija, 1986, 50 lpp. 1879] kodolsintēzes reakcijas mehānisms tika detalizēti izpētīts. Parādīts, ka jau uztveršanas stadijā pēc pilnīgas krītošās daļiņas kinētiskās enerģijas izkliedes veidojas dubultā kodolsistēma un viena kodola nukleoni pakāpeniski, čaumalu pēc čaumalas, tiek pārnesti uz otru kodolu. Tas ir, kodolu apvalka struktūrai ir nozīmīga loma saliktā kodola veidošanā. Pamatojoties uz šo modeli, varēja diezgan labi aprakstīt savienojumu kodolu ierosmes enerģiju un elementu Z = 102–112 veidošanās šķērsgriezumu aukstās saplūšanas reakcijās.
Tādējādi transurāna elementu Z = 107–112 sintēzes progress bija saistīts ar aukstās kodolsintēzes reakciju “atklāšanu”, kurās burvju izotopi 208 Pb un 209 Bi tika apstaroti ar joniem ar Z = 22–30. Kodols, kas veidojas aukstās saplūšanas reakcijā, tiek vāji uzkarsēts un atdziest viena neitrona emisijas rezultātā. Šādi pirmo reizi tika iegūti ķīmisko elementu izotopi ar Z = 107–112. Šie ķīmiskie elementi iegūti laika posmā no 1978. līdz 1998. gadam. Vācijā speciāli uzbūvētā akseleratorā GSI pētniecības centrā Darmštatē. Tomēr turpmāka virzība uz smagākiem kodoliem, izmantojot šo metodi, izrādās sarežģīta, jo palielinās potenciālā barjera starp sadursmju kodoliem. Tāpēc Dubnā tika ieviesta cita metode supersmago kodolu iegūšanai. Tika izmantoti mākslīgi iegūto ķīmisko elementu smagākie izotopi plutonijs Pu (Z = 94), amerīcijs Am (Z = 95), kūrijs Cm (Z = 96), berkelijs Bk (Z = 97) un kalifornijs Cf (Z = 98). kā mērķi. Kalcija izotops 48 Ca (Z = 20) tika izvēlēts kā paātrinātie joni. Atsitiena kodolu separatora un detektora shematisks skats ir parādīts attēlā. 12.11.
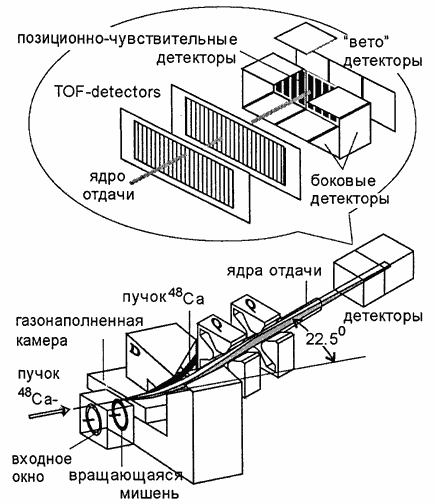
Rīsi. 12.11. Shematisks skats uz atsitiena kodolu separatoru, kur Dubnā tiek veikti supersmago elementu sintēzes eksperimenti.
Atsitiena kodolu magnētiskais separators samazina reakcijas blakusproduktu fonu 10 5 – 10 7 reizes. Reakcijas produkti tika reģistrēti, izmantojot pozīcijai jutīgu silīcija detektoru. Tika izmērīta atsitiena kodolu enerģija, koordinātas un lidojuma laiks. Pēc apstāšanās visiem nākamajiem signāliem no konstatētajām sabrukšanas daļiņām ir jānāk no implantētā kodola apstāšanās punkta. Izveidotā tehnika ļāva ar augstu ticamības pakāpi (≈ 100%) izveidot savienojumu starp detektorā apturētu supersmago kodolu un tā sabrukšanas produktiem. Izmantojot šo tehniku, supersmagie elementi ar
Z = 110–118 (12.2. tabula).
12.2. tabulā parādīti supersmago ķīmisko elementu ar Z = 110–118 raksturlielumi: masas skaitlis A, m - izomēra stāvokļa klātbūtne izotopā ar masas skaitli A, spin-paritāte JP, kodola saistīšanās enerģija Est, īpatnējā saistīšanās enerģija ε, neitronu atdalīšanas enerģijas B n un protonu B p, pussabrukšanas periods T 1/2 un galvenie sabrukšanas kanāli.
Ķīmiskajiem elementiem Z > 112 vēl nav nosaukumu, un tie ir norādīti pieņemtajos starptautiskajos apzīmējumos.
Tabula 12.2
Supersmago ķīmisko elementu raksturojums Z = 110–118
| XX-A-m |
JP |
Svars
kodoli,
MeV |
E St,
MeV |
ε,
MeV |
Bn,
MeV |
Bp,
MeV |
T 1/2 |
Sabrukšanas režīmi |
|---|
| Z = 110 − darmstadtium |
|---|
| Ds-267 |
|
248787.19
|
1934.5
|
7.2
|
|
0.7
|
2,8 ac |
α ≈100% |
| Ds-268 |
0 +
|
249718.08
|
1943.2
|
7.3
|
8.7
|
1.3
|
100 ac |
α
≈
|
| Ds-269 |
|
250650.86
|
1950.0
|
7.2
|
6.8
|
1.3
|
179 ac |
α 100% |
| Ds-270 |
0 +
|
251581.97
|
1958.4
|
7.3
|
8.5
|
|
0,10 ms |
α ≈100%, SF< 0.20%
|
| Ds-270-m |
|
251583.07
|
1957.3
|
7.2
|
|
|
6,0 ms |
α >70%, IT ≤ 30% |
| Ds-271 |
|
252514.72
|
1965.2
|
7.3
|
6.8
|
2.2
|
1,63 ms |
α ≈100% |
| Ds-271-m |
|
252514.72
|
1965.2
|
7.3
|
|
|
69 ms |
IT?, α >0% |
| Ds-272 |
0 +
|
253446.46
|
1973.1
|
7.3
|
7.8
|
2.5
|
1 s |
SF |
| Ds-273 |
|
254380.32
|
1978.8
|
7.2
|
5.7
|
2.5
|
0,17 ms |
α ≈100% |
| Ds-274 |
0 +
|
255312.45
|
1986.2
|
7.2
|
7.4
|
3.0
|
2 s |
α?,
SF? |
| Ds-275 |
|
256246.44
|
1991.8
|
7.2
|
5.6
|
2.9
|
2 s |
α?
|
| Ds-276 |
0 +
|
257178.73
|
1999.1
|
7.2
|
7.3
|
3.2
|
5 s |
SF?,
α?
|
| Ds-277 |
|
258112.63
|
2004.7
|
7.2
|
5.7
|
3.1
|
5 s |
α?
|
| Ds-278 |
0 +
|
259044.92
|
2012.0
|
7.2
|
7.3
|
|
10 s |
SF?,
α?
|
| Ds-279 |
|
259978.62
|
2017.9
|
7.2
|
5.9
|
|
0,18 s |
SF ≈90%,
α ≈10% |
| Ds-281 |
|
261844.60
|
2031.0
|
7.2
|
|
|
9,6 s |
SF ≈100% |
| Z =111 − rentgens |
|---|
| Rg-272 |
|
253452.75
|
1965.5
|
7.2
|
|
0.2
|
3,8 ms |
α ≈100% |
| Rg-273 |
|
254384.34
|
1973.5
|
7.2
|
8.0
|
0.4
|
5 ms |
α?
|
| Rg-274 |
|
255317.74
|
1979.6
|
7.2
|
6.2
|
0.9
|
6,4 ms |
α ≈100% |
| Rg-275 |
|
256249.53
|
1987.4
|
7.2
|
7.8
|
1.2
|
10 ms |
α?
|
| Rg-276 |
|
257183.22
|
1993.3
|
7.2
|
5.9
|
1.5
|
100 ms |
SF?,
α?
|
| Rg-277 |
|
258115.72
|
2000.4
|
7.2
|
7.1
|
1.3
|
1 s |
α?,
SF? |
| Rg-278 |
|
259049.11
|
2006.5
|
7.2
|
6.2
|
1.8
|
4,2 ms |
α ≈100%,
SF |
| Rg-279 |
|
259981.41
|
2013.8
|
7.2
|
7.3
|
1.8
|
0,17 s |
α ≈100% |
| Rg-280 |
|
260914.80
|
2020.0
|
7.2
|
6.2
|
2.1
|
3,6 s |
α ≈100% |
| Rg-281 |
|
261847.09
|
2027.2
|
7.2
|
7.3
|
|
1 m |
α?, SF? |
| Rg-282 |
|
262780.59
|
2033.3
|
7.2
|
6.1
|
2.3
|
4 m |
SF?, α? |
| Rg-283 |
|
263712.98
|
2040.5
|
7.2
|
7.2
|
|
10 m |
SF?, α? |
| Z = 112 − kopernicijs |
|---|
| Cn-277 |
|
258119.32
|
1995.5
|
7.2
|
|
2.2
|
0,69 ms |
α ≈100% |
| Cn-278 |
0 +
|
259051.20
|
2003.1
|
7.2
|
7.7
|
2.8
|
10 ms |
SF?, α? |
| Cn -279 |
|
259984.69
|
2009.2
|
7.2
|
6.1
|
2.7
|
0,1 s |
SF?, α? |
| Cn -280 |
0 +
|
260916.69
|
2016.8
|
7.2
|
7.6
|
3.0
|
1 s |
α?, SF? |
| Cn-282 |
0 +
|
262782.18
|
2030.4
|
7.2
|
|
3.2
|
0,50 ms |
SF ≈100% |
| Cn-283 |
|
263715.57
|
2036.6
|
7.2
|
6.2
|
3.3
|
4,0 s |
α ≥90%, SF ≤10% |
| Cn-284 |
0 +
|
264647.66
|
2044.1
|
7.2
|
7.5
|
3.6
|
101 ms |
SF ≈100% |
| Cn -285 |
|
265580.76
|
2050.5
|
7.2
|
6.5
|
|
34 s |
α ≈100% |
| Z=113 |
|---|
| Uut-278 |
|
|
|
|
|
|
0,24 ms |
α 100% |
| Uut-283 |
|
263719.46
|
2031.4
|
7.2
|
|
1.0
|
100 ms |
α 100% |
| Uut-284 |
|
264652.45
|
2038.0
|
7.2
|
6.6
|
1.4
|
0,48 s |
α ≈100% |
| Uut-285 |
|
265584.55
|
2045.5
|
7.2
|
7.5
|
1.4
|
2 m |
α?, SF? |
| Uut-286 |
|
266517.64
|
2051.9
|
7.2
|
6.5
|
1.4
|
5 m |
α?, SF? |
| Uut-287 |
|
267449.64
|
2059.5
|
7.2
|
7.6
|
|
20 m |
α?, SF? |
| Z=114 |
|---|
| Uuq-286 |
0 +
|
266520.33
|
2048.0
|
7.2
|
|
2.5
|
0,16 s |
SF ≈60%, α ≈40% |
| Uuq-287 |
|
267453.42
|
2054.4
|
7.2
|
6.5
|
2.5
|
0,51 s |
α ≈100% |
| Uuq-288 |
0 +
|
268385.02
|
2062.4
|
7.2
|
8.0
|
2.9
|
0,80 s |
α ≈100% |
| Uuq-289 |
|
269317.91
|
2069.1
|
7.2
|
6.7
|
|
2,7 s |
α ≈100% |
| Z=115 |
|---|
| Uup-287 |
|
267458.11
|
2048.4
|
7.1
|
|
0.5
|
32 ms |
α 100% |
| Uup-288 |
|
268390.81
|
2055.3
|
7.1
|
6.9
|
0.9
|
87 ms |
α 100% |
| Uup-289 |
|
269322.50
|
2063.2
|
7.1
|
7.9
|
0.8
|
10 s |
SF?, α? |
| Uup-290 |
|
270255.30
|
2070.0
|
7.1
|
6.8
|
0.9
|
10 s |
SF?, α? |
| Uup-291 |
|
271187.09
|
2077.7
|
7.1
|
7.8
|
|
1 m |
α?, SF? |
| Z=116 |
|---|
| Uuh-290 |
0 +
|
270258.98
|
2065.0
|
7.1
|
|
1.8
|
15 ms |
α ≈100% |
| Uh-291 |
|
271191.78
|
2071.7
|
7.1
|
6.8
|
1.8
|
6,3 ms |
α 100% |
| Uh-292 |
0 +
|
272123.07
|
2080.0
|
7.1
|
8.3
|
2.3
|
18 ms |
α ≈100% |
| Uh-293 |
|
|
|
|
|
|
53 ms |
α ≈100% |
| Z=117 |
|---|
| Jauns-291 |
|
271197.37
|
2064.9
|
7.1
|
|
-0.1
|
10 ms |
SF?, α? |
| Jauns-292 |
|
272129.76
|
2072.0
|
7.1
|
7.2
|
0.3
|
50 ms |
SF?, α? |
| Z=118 |
|---|
| Uuo-294 |
0 +
|
|
|
|
|
|
1,8 ms |
α ≈100% |
Attēlā 12.12. attēlā parādīti visi zināmie sintēzes reakcijās iegūtie smagākie izotopi ar Z = 110–118, norādot eksperimentāli izmērīto pussabrukšanas periodu. Šeit parādīta arī teorētiski prognozētā stabilitātes salas pozīcija (Z = 114, N = 184).

Rīsi. 12.12. Elementu N-Z diagramma Z = 110-118.
Iegūtie rezultāti nepārprotami liecina par izotopu stabilitātes pieaugumu, tiem tuvojoties divkārši maģiskajam kodolam (Z = 114, N = 184). Pievienojot 7–8 neitronus kodoliem ar Z = 110 un 112, pusperiods palielinās no 2,8 as (Ds-267) līdz ≈ 10 s (Ds-168, Ds 271). Pussabrukšanas periods T 1/2 (272 Rg, 273 Rg) ≈ 4–5 ms palielinās līdz T 1/2 (283 Rg) ≈ 10 min. Elementu Z = 110–112 smagākie izotopi satur ≈ 170 neitronus, kas joprojām ir tālu no maģiskā skaitļa N = 184. Visi smagākie izotopi ar Z > 111 un N > 172 sadalās galvenokārt
α-sabrukšana, spontāna skaldīšanās – retāka sabrukšana. Šie rezultāti labi saskan ar teorētiskajām prognozēm.
vārdā nosauktajā Kodolreakciju laboratorijā. G.N. Flerovs (Dubna) sintezēja elementu ar Z = 114. Reakcija tika izmantota
Kodola 289 114 identificēšana tika veikta, izmantojot α sabrukšanas ķēdi. Izotopa pussabrukšanas perioda eksperimentāls novērtējums 289 114 ~30 s. Iegūtais rezultāts labi saskan ar iepriekš veiktajiem aprēķiniem.
Elementa 114 sintēzes laikā reakcijā 48 Cu + 244 Pu kanālā ar trīs neitronu iztvaikošanu tika novērota maksimālā izotopu iznākums ar Z = 114. Šajā gadījumā savienojuma kodola 289 114 ierosmes enerģija bija 35 MeV.
Teorētiski prognozētā sabrukšanas secība, kas notiek ar 296 116 kodolu, kas veidojas reakcijā 248 Cm + 48 Ca → 296 116, parādīta 12.13.

Rīsi. 12.13. Kodolsabrukšanas diagramma 296 116.
Izotops 296 116 atdziest četru neitronu emisijas rezultātā un pārvēršas par izotopu 292 116, kas pēc tam ar 5% varbūtību divu secīgu e-uztveršanas rezultātā pārvēršas par izotopu 292 114. Rezultātā α sabrukšanas (T 1/2 = 85 dienas ) izotops 292 114 pārvēršas par izotopu 288 112. Izotopa 288 112 veidošanās notiek arī caur kanālu.
No abām ķēdēm iegūtā gala kodola 288 112 pussabrukšanas periods ir aptuveni 1 stunda, un tas sadalās spontānas skaldīšanas rezultātā. Ar aptuveni 10% varbūtību izotopa 288 114 α sabrukšanas rezultātā var veidoties izotops 284 112 Iepriekš minētie periodi un sabrukšanas kanāli tika iegūti ar aprēķinu.
Attēlā 12.14. attēlā parādīta izotopa 288115 secīgu α-sabrukšanas ķēde, kas izmērīta eksperimentos Dubnā. ER ir atsitiena kodola enerģija, kas implantēta pozīcijai jutīgā silīcija detektorā. Var atzīmēt labu sakritību α-sabrukšanas pussabrukšanas periodos un enerģijās trīs eksperimentos, kas norāda uz metodes ticamību supersmago elementu identificēšanai, izmantojot α-daļiņu spektru mērījumus.

Rīsi. 12.14. Izotopa 288115 secīgu α-sabrukšanas ķēde, kas izmērīta eksperimentos Dubnā.
Reakcijā tika sintezēts smagākais laboratorijā ražotais elements ar Z = 118
48 Ca + 249 Cf → 294 118 + 3n.
Pie jonu enerģijām netālu no Kulona barjeras tika novēroti trīs elementa 118 veidošanās gadījumi. Silīcija detektorā tika implantēti 294 118 kodoli un tika novērota secīgu α sabrukšanas ķēde. Šķērsgriezums elementa 118 veidošanai bija ~2 pikobarni. Izotopa 293118 pussabrukšanas periods ir 120 ms.
Attēlā 12.15. attēlā parādīta teorētiski aprēķināta izotopa 293 118 secīgu α-sabrukšanas ķēde un parādīti α-sabrukšanas rezultātā radušos meitas kodolu pussabrukšanas periodi.

Rīsi. 12.15. Izotopa 293 118 secīgu α sabrukšanas ķēde.
Ir doti α-sabrukšanas rezultātā izveidoto meitas kodolu vidējie mūži.
Analizējot dažādas iespējas supersmago elementu veidošanās reakcijās ar smagajiem joniem, jāņem vērā šādi apstākļi.
- Ir nepieciešams izveidot kodolu ar pietiekami lielu neitronu skaita attiecību pret protonu skaitu. Tāpēc par krītošo daļiņu ir jāizvēlas smagie joni ar lielu N/Z.
- Ir nepieciešams, lai iegūtajam saliktajam kodolam būtu zema ierosmes enerģija un mazs leņķiskais impulss, jo pretējā gadījumā skaldīšanas barjeras efektīvais augstums samazināsies.
- Ir nepieciešams, lai iegūtajam kodolam būtu sfēriska forma, jo pat neliela deformācija izraisīs supersmagā kodola ātru sadalīšanos.
Ļoti daudzsološa metode supersmago kodolu iegūšanai ir tādas reakcijas kā 238 U + 238 U, 238 U + 248 Cm, 238 U + 249 Cf, 238 U + 254 Es. Attēlā 12.16. attēlā parādīti aprēķinātie šķērsgriezumi transurāna elementu veidošanās gadījumā, apstarojot 248 Cm, 249 Cf un 254 Es mērķus ar paātrinātiem 238 U joniem. Šajās reakcijās jau ir iegūti pirmie rezultāti par šķērsgriezumiem elementu veidošanai ar Z > 100 Lai palielinātu pētāmo reakciju iznākumu, mērķa biezumi tika izvēlēti tā, lai reakcijas produkti paliktu iekšā mērķis. Pēc apstarošanas atsevišķi ķīmiskie elementi tika atdalīti no mērķa. Vairāku mēnešu laikā iegūtajos paraugos tika reģistrēti α-sabrukšanas produkti un dalīšanās fragmenti. Dati, kas iegūti, izmantojot paātrinātos urāna jonus, skaidri norāda uz smago transurāna elementu iznākuma pieaugumu salīdzinājumā ar vieglākiem bombardējošiem joniem. Šis fakts ir ārkārtīgi svarīgs, lai atrisinātu supersmago kodolu saplūšanas problēmu. Neskatoties uz grūtībām strādāt ar atbilstošiem mērķiem, prognozes par virzību uz augstu Z izskatās diezgan optimistiskas.

Rīsi. 12.16. Šķērsgriezumu aprēķini transurāna elementu veidošanās reakcijās 238 U ar 248 Cm, 249 Cf un 254 Es
Sasniegumi supersmago kodolu jomā pēdējos gados ir bijuši satriecoši iespaidīgi. Tomēr visi mēģinājumi atklāt Stabilitātes salu līdz šim ir bijuši nesekmīgi. Viņa meklēšana turpinās intensīvi.
Atomu kodolu apvalka struktūrai ir nozīmīga loma supersmago kodolu stabilitātes palielināšanā. Maģiskie skaitļi Z ≈ 114 un N ≈ 184, ja tie patiešām pastāv, var izraisīt ievērojamu atomu kodolu stabilitātes pieaugumu. Būtiski ir arī tas, ka supersmago kodolu sabrukšana notiks α-sabrukšanas rezultātā, kas ir svarīgi eksperimentālo metožu izstrādei jaunu supersmago kodolu noteikšanai un identificēšanai.
|
Ķīmijterapijas “ķīmiskais laikmets” sākās ar attīstību
apstrādes rūpniecība. Izcila analīze
Markss un Ļeņins parāda, kā šis process notika
kapitālisma attīstība rūpniecībā: no vienkāršas sadarbības
darbaspēks caur ražošanas (16.-7.gs.) rūpniecību
18. gadsimta beigās un 19. gadsimta sākumā pārgāja uz kapitālistisko
rūpnīca, t.i., liela mēroga mašīnu ražošana.
Roku darbs tika aizstāts ar mašīnu darbu.
Tvaika dzinēji, dzelzceļa un ūdens transporta attīstība
tvaika transportēšana, mašīnu vērpšana, jaunas metodes
čuguns un tērauds - tas viss izraisīja revolūciju rūpniecībā.
Ir pienācis industriālās revolūcijas laikmets.
Ķīmijas zinātne tik tikko spēja sekot mehāniskās zinātnes prasībām
nozare. Teorijas jomā šī zinātne ir radījusi
liels lēciens uz priekšu 18. gadsimta vidū.
Zinātniskās ķīmijas un termodinamikas pamatus lika mūsu
slavenais tautietis Lomonosovs.
1748. gadā slavenajā vēstulē matemātiķim Eileram, Krievijas Zinātņu akadēmijas loceklim, Lomonosovs pirmo reizi formulēja
matērijas un kustības noturības likums. Viņš
pieder pie otra svarīgākā nopelna: viņš paaugstināja
ideja par nepieciešamību izpētīt atomu un
vielas molekulārā struktūra, jo
visu ķermeņu īpašības, to ķīmiskā un fiziskā būtība.
≪ ...ķīmija,” rakstīja Lomonosovs savā Vārdā par ķīmijas priekšrocībām,
Pirmais līderis būs iekšējā atklāšanā
ķermeņu zāles, pirmie iekļūstot iekšējās slēptuvēs
korpuss, pirmais ļaus iepazīties ar daļām un ≫ .
≪ Ķīmija plaši izstiepj rokas cilvēku lietās
≫ - ar šo vārdu viņš beidza vienu no šī raksta sadaļām
≪Vārdi≫. ≪ Pietiek ar nepārtrauktu ķermeņu piedzimšanu un iznīcināšanu
daiļrunīgi runā par asinsķermenīša kustību≫, rakstīja
miruši, pārvietoties augos - dzīvos un mirušos, minerālos
vai neorganiskajā, tātad it visā≫.
Aušanas ražošanas mehanizācija radījusi nepieciešamību
revolūcijas kalikona drukāšanas un krāsošanas mehānikā un ķīmijā
uzņēmējdarbība, metālu apstrāde, nepieciešama to rūdīšana
dziļa ķīmisko elementu iejaukšanās procesā
Neapšaubāmi mūsdienu ķīmijas galvenie sasniegumi
zinātne ir parādā trim izciliem krievu ķīmiķiem - Nikolajam
Nikolajevičam Zininam, Aleksandram Mihailovičam Butlerovam I
Dmitrijs Ivanovičs Mendeļejevs.
Kazaņas universitātes profesors N. N. Zinins 1841. gadā
ko iegūst ķīmiskās sintēzes ceļā no cikliska savienojuma
nitrobenzolanilīns ir izejprodukts, no kura
Apstrādājot, tiek iegūti desmitiem dažādu krāsvielu.
Pirms tam krāsas tika gatavotas no augu produktiem.
Zinins pamatoti tiek uzskatīts par tēvu t.s
sintētiskā ķīmija.
Ja Zinins neko vairāk nebūtu darījis kā pārveidojis
nitrobenzolu anilīnā, tad viņa vārds būtu iekļauts
zinātnes vēsture kā lielākā ķīmiķa vārds. Anilīna sintēze
atklāja jaunu ēru ķīmiskajā un medicīnas nozarē.
Apstrādājot anilīnu ar sālsskābi, metilspirtu,
fosgēns un citi reaģenti, jūs varat iegūt ļoti
liels skaits krāsvielu audumiem. Vairāk nekā divi simti krāsvielu
ražoja padomju ķīmiskā rūpniecība no
bezkrāsains anilīns. Ražošanā izmanto anilīnu
filmas, kā arī krāsu filmu izstrādātāji. No anilīna
ražo vielu, kas paātrina vulkanizācijas procesu
gumija. Ražots vairāk nekā simts narkotiku
pašlaik, ieskaitot streptocīdu un sulfonamīdus,
ir anilīna atvasinājumi.
18. gadsimtā Lomonosova skaidrais prāts paredzēja nozīmi
ķīmija medicīnai: ≪ Ārsts bez pietiekamām zināšanām ķīmijā
nevar būt ideāls...≫ ; ≪ cerība tikai no ķimikālijām
iespējams labot medicīnas zinātnes nepilnības...≫ .
gadā Zinina pēctecis A.M. Butlerovs veica revolūciju
organisko ķīmisko savienojumu uzbūves doktrīna.
Pārliecināts par atomu realitāti, Butlerovs izvirzīja mērķi
izteikt ķīmiskās saites starp atomiem precīzās formulās,
veidojot organiska savienojuma molekulu. Butlerovs
uzskatīja, ka, izmantojot, ir iespējams noskaidrot molekulu struktūru
fizikālās metodes un ķīmiskās transformācijas.
Sekojot šim ceļam, viņš izstrādāja savu ķīmijas teoriju
organisko savienojumu struktūra. Pēc neatlaidīgiem eksperimentiem
ar butilspirtiem Butlerovs konstatēja, ka viens un
vienāds noteiktu atomu skaits (piemēram, oglekļa,
ūdeņradis un skābeklis), kas atrodas ķēdē,
var ražot dažādus produktus un kādas ir iegūto īpašības
ķīmiskie produkti ir atkarīgi no secības, kādā tie būs
elementi ir savienoti viens ar otru. Tas pieauga kā cipars
iespējamās kombinācijas jaunu ķīmisko vielu sintēzē,
un saņemto medikamentu skaits
ķīmiskās sintēzes ceļā.
Lielākais 19. gadsimta atklājums ir periodiskais likums
Mendeļejevs -. noveda pie stingras kārtības nodibināšanas un
ķīmisko elementu modeļi. Šīs mērs
atomu svars kļuva par modeli. Daudzas ķīmijterapijas zāles
pagātnē tika atklāti nejauši. Bet zinātne ir nejaušības ienaidnieks.
Zinātnes atziņām attīstoties, daudzas lietas šķita noslēpumainas
un nesaprotams, kļuva skaidrs un likumsakarīgs.
Mendeļejeva periodiskais likums ielika visu ķīmisko
zinātne un jo īpaši ķīmijterapija uz stabila zinātniska pamata.
"Pirms periodiskā likuma," rakstīja Mendeļejevs, ". vienkārši
ķermeņi pārstāvēja tikai fragmentāras, nejaušas parādības
daba: nebija pamata gaidīt jaunus, bet atkal
atrasti to īpašumos bija pilnīgs negaidīts jaunums.
Periodiskā likumība bija pirmā, kas to padarīja iespējamu
redzēt elementus, kas vēl nav atklāti tādā attālumā, ka tas nav iespējams
ķīmiskā redze, kas bruņota ar šo modeli, līdz
poras nesasniedza, un tajā pašā laikā jauni elementi, kas tika atklāti iepriekš,
tika uzzīmēti ar daudzām īpašībām ≫ 1.
Nav brīnums, ka Engelss raksturoja zinātnisko tālredzību
Mendeļejevs kā zinātnisks varoņdarbs. Tas bija patiesi izcils
uzvara ķīmisko parādību zinātnei, uzvara, kas ļāva
cilvēcei iet ilgstošu atbrīvošanās ceļu
no nejaušības spēka un dabas spēku pakļaušanas. Periodiski
Periodiskā sistēma ļāva atrast veselumu
ķīmisko elementu grupa tuvu viens otram, noderīga
daudzu slimību ārstēšanai (arsēns, dzīvsudrabs, antimons).
Šie elementi zinātniekiem parādījās 19. gadsimta beigās kā
būtu zelta raktuves. Tajā pašā laikā zinātnieki pilnībā izmantoja
Zinina ķīmiskās sintēzes princips un Butlerova kombinācijas
atomu un molekulu izkārtojumā.
Starp medicīnas zinātniekiem, kas nodarbojas ar sintētikas ražošanu
narkotikas, vislielākie panākumi bija Ērliham.
Visa Ērliha dzīve bija veltīta neatlaidīgai īstenošanai
viena ideja - iegūta ar ķīmisku savienojumu
nekaitējot ķermenim.
Svarīgi uzsvērt, ka šī ideja tika pausta 1891. gadā
ķīmijterapijas dibinātājs D. L. Romanovskis. Viņš rakstīja,
ko viņš uzskata par ideālām zālēm ≪ vielu, kas
injekcija slimā ķermenī radīs vismazāko kaitējumu
pēdējā un izraisīs vislielākās postošās pārmaiņas
kaitīgais līdzeklis≫. Romanovskis paredzēja Ērlija ideju
ha par “burvju lodēm”, kas viegli trāpa ienaidniekiem. Romanovskis
bija pirmais, kurš, pamatojoties uz precīziem novērojumiem, izveidoja
svarīgākais ķīmijterapijas likums ir tiešais darbības mehānisms
ķīmiskās zāles pret slimības izraisītāju.
≪ Hinīns, pietiekamā daudzumā ievadot malārijas pacienta organismā
viegli novērojamas destruktīvas izmaiņas, galvenokārt
attēls - tā būtība, kāpēc šis līdzeklis jāuzskata par patiesu
specifiskas zāles pret malāriju≫.
tiek atspoguļota šī malārijas līdzekļa specifika - patiesā iedarbības specifika uz pašu slimības būtību,
Romanovskis pirmais izvirzīja jautājumu par ≪ radikālu rīcību
≫ ķīmijterapijas zāles patogēniem vai, kā viņš teica,
≪ ražotāju≫ slimība. Tātad viņš bija iniciators
idejas lieliskai sterilizācijas terapijai.
Ja hinīns eksistē dabā, pamatoti pēc
cilvēka ķermenim, tad ir jābūt citiem
līdzīgas vielas, ko var izmantot, lai uzveiktu citas slimības.
19. gadsimta beigās ķīmijas zinātne turpināja savu attīstību
Lomonosova iesāktais un pabeigtais triumfa gājiens
Zinins, Butlerovs un Mendeļejevs.
Žurnāli bija piepildīti ar jauniem un interesantiem
ziņojumi par ķīmijas iekarošanu.
Tomēr ar ko sākt? Kura viela no jau iegūtajiem simtiem
ķīmiski var izmantot sintēzei
ķīmijterapija?
Vēl būdams students, Ērlihs atkārtoja labi zināmo eksperimentu
Kijevas profesors Geibels, kurš to pierādīja, kad
Svina saindēšanās gadījumā šis metāls ir nevienmērīgi sadalīts
organismā: dažos orgānos svins uzkrājas manāmi
daudzumos, bet to nevar atklāt līķī pat ar vissmalkākajiem
reaģenti. Tas nozīmē, ka ķīmiskajām vielām ir
selektīva darbība, Ērlihs nolēma.
Tomēr Ērlihs atteicās no eksperimentiem ar svinu, jo
Acīs saindētās šūnas ne ar ko neatšķīrās no veselajām.
Viņš apmetās uz metilēnzilo krāsu, jo tā
būs ērtāk novērošanai, un ieteica ārstēt malāriju
metilēnzils. Šī ārstēšana deva dažus rezultātus.
Ērlihu viņi iedrošināja un sāka paplašināt savus eksperimentus.
šaura lapa ar asti un atgādina zirgus
pelēm un izraisīja tām letālu slimību.
Erlihs apsēdās laboratorijā un sāka pārbaudīt krāsas
inficētas peles. Tas, iespējams, bija vienkāršots veids,
bet tie bija pirmie zinātniskās ķīmijterapijas soļi. Grūti
nekavējoties noteikt, kāda krāsa ir dzīvnieku apstākļos
Viena krāsa padarīja peles šenilu, otra padarīja tās dzeltenas un
astes tripanosomas joprojām peldēja asinsritē
pelēm un tās nogalināja. Ar krāsām nekas neiznāca.
Dabaszinātnēs dzimst “zelta patiesības graudi”.
no ≪ tūkstošiem tonnu apstrādātas rūdas≫. Jums tas vienkārši jāatver
jebkuru līdzekli, un tad ķīmiķis to sadalīs, pievieno
skābi vai sārmu, apvieno ar reaģentiem, nosaka atomu
svaru, pārbaudīs uz slimiem dzīvniekiem un pēc tam uz cilvēkiem...
Un tad terapeitisko ķīmijterapijas zāļu tabulā parādās
jauns dzīvības glābšanas līdzeklis.
Bija grūti tikt līdz racionālai ķīmijterapijai.
Bija jāmeklē kompass, kam būtu jānoved pie pareizā
ceļš. Bija jāmeklē raksti...
Un tad kādu dienu, sēžot savā kabinetā, Erlihs lasīja
jaunākais ķīmiskā žurnāla numurs par jaunu patentētu
nozīmē. To sauca par "atoksilu", kas nozīmē netoksisks.
Ir sākta šo zāļu pārbaude pelēm, kas inficētas ar
tripanosomas.
Pēc simtiem eksperimentu varēja atzīmēt, ka atoksil
faktiski ārstē peles.
Bet dažas peles joprojām nomira. Tāpēc nē
Tātad atoksils jau ir nekaitīgs.
Ērlihs nolēma to padarīt nekaitīgu. Šis produkts bija vērts
lai pie tā strādātu.
Atoksils saturēja tādu pašu benzola gredzenu kā
un dažās krāsās.
Benzola gredzens ir seši oglekļa atomi, kas saistīti kopā.
vienā lokā. Bet tam tika pievienots arsēna oksīds.
Tas, protams, padarīja narkotiku dziedināšanu. Arsēns - zināms
inde, bet kombinējot ar benzola gredzenu
Izrādījās, ka tās ir ķīmijterapijas zāles.
Tomēr vajadzēja šo indi vairāk “cilvēcināt”, pagriežot
to padarītu vēl drošāku un tajā pašā laikā jaudīgāku
līdzeklis pret patogēniem.
atoksilu, viņi teica, ka nav iespējams mainīt atoksilu, tas ir tieši tur
sabruks. Tomēr Ērliham izdevās modificēt šīs zāles
simtiem arsēna preparātu, netraucējot
benzola un arsēna kombinācijas.
Viņš strādāja savā laboratorijā divus gadus, līdz viņš
atklāja līdzekli, kas pilnībā attīra asinis
pelēm no mežonīgajām tripanosomām, kas tās nogalināja. Tajā pašā laikā jauns
Produkts izrādījās nekaitīgs pelēm. Viņi to labi panesa
≪ 606≫ vai salvarsāns, tas bija jaunās zāles nosaukums,
jo viņš bija 606. atoksila variants. Šīs zāles bija
vislabākās ķīmiskās sintēzes produkts un tā sagatavošana
bija saistīts ar sprādziena un ugunsgrēka draudiem
liels skaits savienojumu, kas piedalās reakcijā
ēteriskie tvaiki.
Un pats galvenais, bija iespējams konstatēt, ka zāles ir vajadzīgas
uzglabāt bezgaisa ampulā - gaisa piejaukums padara
tā indīga.
Šīs bija zāles, kurām bija ķīmiskais nosaukums: dioc-
Si-diamino-arsenobenzol-dihidrohlorīds.
Bet tad notika viens nozīmīgs notikums.
Īsi pirms Ērliha pētījumiem slavenais zinātnieks Šovs.
Dīns atklāja sifilisa izraisītāju spirohetu pallidum, kas notiek
no tripanosomu ģimenes.
Bet, Erlihs domāja, jūs nevarat apstāties pie zirgiem
tripanosomas, ir nepieciešams ietekmēt spirohetu,
kas ietekmē cilvēku.
Tomēr viņš uzreiz nepārgāja uz cilvēkiem; viņš inficējās ar sifilisu
trušiem un pēc tam tos ārstēja ar zālēm ≪ 606≫. Pēc
pēc vairākām infūzijām trušiem vairs nebija neviena
spirohetas. Zāļu devas tika izstrādātas arī trušiem.
Ērlihs ražoja vēl 308 savienojumus un ieguva pilnīgāku
zāles -≪ 914≫ (neosalvarsāns). Šīs zāles
izšķīdina 5 kubikcentimetros ūdens. Viņa ievads
ķermenī izrādījās vēl drošāks: bija reakcijas
Zāles joprojām saglabāja dažas toksiskas īpašības.
Dažiem pacientiem, īpaši, ja tiek ievadītas lielas devas,
zāles ≪ 606≫ un ≪ 914≫ izraisīja smadzeņu iekaisumu,
apziņa, drudzis, ādas asiņošana.
Ērliha ienaidnieki sacēla traci par jaunajām zālēm.
Viņi Erliham sagādāja daudz nepatikšanas.
Kad Ērliha narkotikas tika pārbaudītas lielā skaitā
pacientiem, izrādījās, ka tiem ir toksiska iedarbība
ārkārtīgi reti.
Visa pasaule ir atzinusi jaunu rīku milzīgo nozīmi.
Sifiliss vairs nav briesmīga slimība. Ārstēšana deva
izcili rezultāti; pēc tam pacientiem čūlas pazuda
vairākas infūzijas.
Ērlihs nolēma likvidēt recidivējošā drudža spirohetu,
kas saistīti ar sifilītu spirohetu.
Šajā laikā dažās Krievijas pilsētās tas tika novērots
recidivējoša drudža uzliesmojumi. Krievu ārsti Yu Iversen
Pēterburga un P.K. Gallers Saratovā pieņēma drosmīgu lēmumu
un pirmais pasaulē izveidoja plašu jauno testu
zāles pacientiem ar recidivējošu drudzi.
Ārstēšanas efekts bija pārsteidzošs: pēc pacienta
40° temperatūrā iebēra pusgramu Ērliha
zāles, pēc 14-6 stundām sākās spēcīgākie sviedri un
temperatūra pilnībā nokritās. Pacients pilnībā atveseļojās.
Viņa ķermenis tika pilnībā atbrīvots no spirohetām.
Vai tas nav zinātnieku sapņu piepildījums par lielisku sterilizāciju
Pēc vairāku gadu ilgas salvarsāna lietošanas krievu zinātnieki
konstatēja, ka pēc salvarsāna uzlējumiem ir
tikai nelielas reakcijas, bet rodas letālas komplikācijas
ārkārtīgi reti (viena nāve uz 100 000 infūzijām).
Zāļu kvalitātes uzlabošana, pareizas noteikšana
devas un precīzas kontrindikācijas, rakstīja 1916.-917
gados mūsu zinātnieki G.I., Bogrovs un V.V.
jauns - novedīs pie tā, ka šis līdzeklis būs pilnībā
droši.
Progresīvie krievu ķīmiķu pētnieki un ārsti drīzumā
pēc Ērliha atklājuma viņi izvirzīja sev uzdevumu ražot
iekšzemes salvarsāns.
Ķīmiķis V. A. Smirnovs V. K. Fereina farmācijas laboratorijā
Jau 1914. gadā labs, netoksisks veida zāles
salvarsana. Tās vienīgais trūkums bija nedaudz samazināts
peles, ko ražoja G. Šereševskis, S. L. Bogrovs,
S. S. Usoltsev et al., jaunas zāles, kas tika nosauktas ≪ ben-
Zarsan≫ sāka lietot klīnikās pacientu ārstēšanai. Profesors
T. P. Pavlovs, G. I. Meščerskis un V. V. Ivanovs vairākos publicētajos rakstos
1916-917 “Krievu ārsts”, “Medicīnas Avīzē” un
≪Krievijas žurnāls par ādas un veneriskām slimībām≫, viņi sniedza informāciju par pirmo krievu
salvarsana lielisks apskats.
Pēc tam no 1916. gada tika organizēta masveida rūpnīcu ražošana
krievu salvarsāna ražošana. Šo iestudējumu vadīja slavenais
Krievu ķīmiķis P. F. Ryumshin, kurš izstrādāja vispārpieņemto oriģinālu
salvarsāna sintēzes tehnoloģija.
Vienlaikus ar Smirnovu, krievu salvarsan (ar nosaukumu ≪ ar-
Ol≫) 1914. gadā sintezēja Maskavas ķīmiķi I. I. Ostromyslen-
skiy un S.S. Kelbasinsky.
1915. gadā “Krievijas žurnālā par ādas un veneriskajām slimībām”
par to bija ļoti labvēlīga Bogrova un Meščerska atsauksme
narkotiku.
Pēc Lielās oktobra sociālistiskās revolūcijas tā tika izveidota
Krievijas salvarsāna (novarsalan, novarsol) ražošana rūpnīcā
Divdesmitajā gadsimtā periodiskās tabulas galveno apakšgrupu elementi bija mazāk populāri nekā tie, kas atradās pakārtotajās apakšgrupās. Litijs, bors un germānija atradās savu dārgo kaimiņu — zelta, pallādija, rodija un platīna — ēnā. Protams, jāatzīst, ka galveno apakšgrupu elementu klasiskās ķīmiskās īpašības nav salīdzināmas ar ātrajiem un elegantajiem procesiem, kuros piedalās pārejas metālu kompleksi (par šo reakciju atklāšanu ir piešķirta ne viena vien Nobela prēmija) . Septiņdesmito gadu sākumā ķīmiķu vidū bija vispārējs uzskats, ka galveno apakšgrupu elementi jau ir atklājuši visus savus noslēpumus un viņu izpēte patiesībā bija laika izšķiešana.
Slēptā ķīmiskā revolūcija
Kad šī raksta autors bija students (1992. gadā ieguva diplomu Kazaņas Universitātē), viņš un daudzi viņa kursabiedri studēja ķīmiju lpp-elementi šķita garlaicīgākā sadaļa. (Atcerieties to s-, lpp- Un d-elementi ir tie, kuru valences elektroni ir attiecīgi aizņemti s-, lpp- Un d-orbitāles.) Mums stāstīja, kādā veidā šie elementi eksistē zemes garozā, tika mācītas to izdalīšanas metodes, fizikālās īpašības, tipiskie oksidācijas stāvokļi, ķīmiskās īpašības un praktiskie pielietojumi. Tas bija divtik garlaicīgi tiem, kuri gāja cauri ķīmijas olimpiādēm un visu šo noderīgo informāciju uzzināja jau skolnieka vecumā. Varbūt tāpēc mūsu laikos neorganiskās ķīmijas katedra nebija īpaši populāra, izvēloties specializāciju - visi centāmies nokļūt pie organisko vai organoelementu speciālistiem, kur viņi runāja par ķīmijā ienākušo pārejas metālu laikmetu, katalizējot visu iespējamo. un neiedomājamas vielu pārvērtības.
Tolaik nebija ne datoru, ne interneta, visu informāciju saņēmām tikai no abstraktiem žurnāliem par ķīmiju un dažiem ārzemju žurnāliem, kurus abonēja mūsu bibliotēka. Ne mēs, ne mūsu skolotāji nezinājām, ka 80. gadu beigās jau bija manāmas pirmās renesanses pazīmes galveno apakšgrupu elementu ķīmijā. Toreiz viņi atklāja, ka ir iespējams iegūt eksotiskas formas lpp-elementi - silīcijs un fosfors vāji koordinētā un mazoksidētā stāvoklī, bet tajā pašā laikā spēj veidot savienojumus, kas ir diezgan stabili istabas temperatūrā. Lai gan toreiz netika runāts par to praktisko izmantošanu, pirmie veiksmīgie šo vielu sintēzes piemēri liecināja, ka galveno apakšgrupu elementu ķīmija ir nedaudz novērtēta un, iespējams, pienāks laiks, kad lpp-elementi varēs izcelties no ēnām d- un pat f- elementi. Galu galā tas notika.
1981. gadu var uzskatīt par sākumpunktu pagriezienam uz galveno apakšgrupu elementiem. Toreiz tika publicēti pat trīs raksti, kas atspēko domu, ka stabila dubultā vai trīskāršā saite var veidoties tikai tad, ja viens no šīs ķīmiskās saites partneriem (vai vēl labāk, abi) ir otrā perioda elements. Šo “dubulto saišu likumu” pirmais atspēkoja Roberts Vests no Viskonsinas universitātes, kura grupā viņi pirmie sintezēja stabilu silēnu, savienojumu ar silīcija-silīcija dubultsaiti, smagāku alkēnu analogu, kas pazīstams visiem. no organiskās ķīmijas ( Zinātne, 1981, 214, 4527, 1343–1344, doi: 10.1126/zinātne.214.4527.1343). Neilgi pēc tam Tokijas universitātes pētnieki, kas strādāja Masaaki Yoshifuji vadībā, ziņoja par savienojuma sintēzi ar fosfora-fosfora dubultsaiti ( , 1981, 103, 15, 4587–4589; doi:10.1021/ja00405a054). Tajā pašā gadā Gerds Bekers no Štutgartes universitātes spēja iegūt stabilu fosfalkīnu, savienojumu ar fosfora-oglekļa trīskāršo saiti, ko var uzskatīt par fosforu saturošu karbonskābes nitrilu analogu ( Zeitschrift für Daturforschung B, 1981, 36, 16).

Fosfors un silīcijs ir trešā perioda elementi, tāpēc neviens no tiem negaidīja šādas iespējas. Pēdējā savienojumā fosfora atoms ir koordinatīvi nepiesātināts, un tas ļāva mums cerēt, ka tas vai tā analogi tiks izmantoti kā katalizatori. Iemesls cerībām bija tas, ka katalizatora galvenais uzdevums ir kontaktēties ar substrāta molekulu, kas jāaktivizē, to spēj tikai tās molekulas, kurām reaģents var viegli pietuvoties, un lielākajai daļai ķīmiķu pazīstamajos fosfātos — fosfora atoms; , ko ieskauj četras grupas, to nekādā gadījumā nevar saukt par pieejamu centru.
Galvenais ir tilpuma vide
Visas trīs sintēzes, kas publicētas 1981. gadā, izdevās, jo aizvietotāji, kas apņem galvenos apakšgrupas elementus to jaunajos, eksotiskajos savienojumos, tika izvēlēti pareizi (pārejas metālu ķīmijā aizvietotājus sauca par ligandiem). Jaunajiem West, Yoshifuji un Becker iegūtajiem atvasinājumiem bija viena kopīga iezīme - lielgabarīta ligandi, kas saistīti ar galveno apakšgrupu elementiem, stabilizēja silīciju vai fosforu vāji koordinētā stāvoklī, kas citos apstākļos nebūtu stabils. Lielapjoma aizvietotāji aizsargā silīciju un fosforu no gaisā esošā skābekļa un ūdens, kā arī neļauj tiem iesaistīties disproporcijas reakcijā un iegūt tipiskos oksidācijas stāvokļus (attiecīgi +4 un +5 silīcijam un fosforam) un koordinācijas skaitļus (četri abi elementi). Tādējādi silēnu stabilizēja četras lielapjoma mezitilgrupas (mezitils ir 1,3,5-trimetilbenzols), bet fosfaalkīnu ar apjomīgu terc-butila aizvietotāju.
Kad kļuva skaidrs, ka lielgabarīta ligandi stabilizē savienojumus, kuros lpp-elementi ir zemā oksidācijas pakāpē un/vai ar zemu koordinācijas skaitli, citi zinātnieki sāka iesaistīties jaunu, neparastu galveno apakšgrupu elementu atvasinājumu iegūšanā. Kopš 2000. gadiem gandrīz katrā numurā Zinātne(un kopš žurnāla parādīšanās 2009. gadā Dabas ķīmija- gandrīz katrā numurā) tiek ziņots par kādu eksotisku kombināciju ar galveno apakšgrupu elementu.

Tādējādi vēl nesen neviens nevarēja iedomāties, ka izdosies iegūt un raksturot stabilus sililēnus – silīciju saturošus karbēnu ekvivalentus.
Karbēni ir ļoti reaģējošas sugas, kurās divvērtīgajam un divkārši koordinētajam oglekļa atomam ir elektronu pāris (stabilāks vienkarbēns) vai divi atsevišķi nepāra elektroni (reaktīvāks trīskāršais karbēns). 2012. gadā Kamerons Džounss no Austrālijas Monašas universitātes un viņa kolēģi no Oksfordas un Londonas Universitātes koledžas aprakstīja pirmo sililēnu, kurā ir divvērtīgais silīcijs, kuru stabilizē apjomīgs bora ligands ( Amerikas Ķīmijas biedrības žurnāls, 2012, 134, 15, 6500–6503, doi: 10.1021/ja301042u). Sililēnu var izolēt kristāliskā stāvoklī, un ir vērts atzīmēt, ka tas saglabājas stabils temperatūrā līdz 130°C. Bet šķīdumā karbēna silīcija analogs dimerizējas, veidojot silēnu vai tiek ievadīts alkānu C-H saitēs, atveidojot tā karbēna analogu ķīmiskās īpašības.
Ķīmiķi turpina iegūt jaunus organiskos savienojumus, kas satur galveno apakšgrupu elementus. Jo īpaši viņi mēģina aizstāt otrā perioda elementu labi zināmā struktūrā ar līdzīgu senāka perioda elementu (šajā Chemoscope numurā ir runa par fosforu saturoša analoga sagatavošanu vienai no pirmajām sintezētajām organiskajām vielām. vielas). Cits virziens ir nedaudz līdzīgs reto pastmarku kolekcionēšanai, tikai pastmarku vietā ir ķīmiskas struktūras. Piemēram, 2016. gadā Aleksandrs Hincs no Oksfordas mēģināja iegūt ciklu, kas satur četru dažādu pnitogēnu atomus (galvenās apakšgrupas 5. grupas elementi no slāpekļa līdz bismutam). Viņam neizdevās pilnībā atrisināt problēmu - molekula ar lineāru struktūru nenoslēdzās ciklā. Tomēr iespaidīga ir arī molekula ar unikālu Sb-N-As = P ķēdi, ieskaitot četras no piecām. lpp-slāpekļa apakšgrupas elementi ( Chemisrty. Eiropas žurnāls, 2016, 22, 35, 12266–12269, doi: 10.1002/chem.201601916).

Protams, nevar runāt par galveno apakšgrupu elementu eksotisko atvasinājumu sintēzi tikai kā par “ķīmisko savākšanu”, jo labi zināmu organisko savienojumu analogu iegūšana, kas satur senāku periodu elementus, noteikti ir svarīga struktūras teoriju noskaidrošanai. no ķīmiskajām saitēm. Protams, tas nav vienīgais iemesls ķīmiķu interesei. Vēlme atrast jomas, kurās šīs vielas var izmantot praksē, ir tieši iemesls galveno apakšgrupu elementu ķīmijas renesansei.
Vēl 80. gados, pēc pirmo vielu sintēzes, kurās tika novērota zema koordinācija lpp-elementi, ķīmiķi cerēja, ka šādi koordinatīvi nepiesātināti savienojumi spēs katalizēt daudzas reakcijas tāpat kā pārejas metālu kompleksi. Būtu ļoti vilinoši apmainīt dārgos platīna un pallādija savienojumus pret molekulām, kas satur tikai galveno apakšgrupu elementus. Informācija par neparastu savienojumu īpašībām, kas parādījās jau šajā tūkstošgadē lpp-elementi apstiprināja teorētiskās prognozes. Izrādījās, ka daudzi no tiem aktivizē ogļūdeņražus, molekulāro ūdeņradi un oglekļa dioksīdu.
Kāpēc pārejas metāli ir slikti?
Šķiet, kāpēc izstrādāt jaunus katalizatorus procesiem, kurus jau sen ir lieliski paātrina pārejas metālu atvasinājumi? Turklāt pārejas elementu metālorganiskā ķīmija nestāv uz vietas – visu laiku tiek atklāti jauni reaktivitātes aspekti. d- elementi. Bet cēlajiem pārejas metāliem ir savi trūkumi. Pirmkārt, cena: visefektīvākie katalizatori organisko un organoelementu savienojumu pārveidošanai ir rodija, platīna un pallādija kompleksi. Otrā grūtība ir platīna un pallādija dabisko rezervju izsīkšana. Visbeidzot, vēl viena problēma ar platīna vai pallādija katalizatoriem ir augsta toksicitāte. Tas jo īpaši attiecas uz narkotiku iegūšanu, jo to cenu ievērojami palielina izmaksas, kas saistītas ar vielas attīrīšanu pat no pārejas metālu nelieliem daudzumiem. Pāreja uz jauniem katalizatoriem vismaz ievērojami samazinās ārstnieciskās vielas izmaksas un, iespējams, vienkāršos mērķa reakcijas produkta attīrīšanu.
Ir papildu priekšrocības, ko var nodrošināt katalizatoru izmantošana, pamatojoties uz galveno apakšgrupu elementiem. Tādējādi ir iespējams, ka dažas zināmas reakcijas notiks maigākos apstākļos, kas nozīmē, ka būs iespējams ietaupīt enerģiju. Piemēram, 1981. gadā savā darbā par pirmā silēna sintēzi un īpašībām Džonss pierādīja, ka savienojums ar silīcija-silīcija dubultsaiti var aktivizēt ūdeņradi temperatūrā, kas ir pat zemāka par istabas temperatūru, turpretim esošajiem rūpnieciskajiem hidrogenēšanas procesiem ir nepieciešams augstas temperatūras izmantošana.
Viens no svarīgākajiem ķīmiskajiem procesiem, kas atklāts jaunajā tūkstošgadē, ir molekulārā ūdeņraža aktivizēšana ar digermīna palīdzību, kas ir germāniju saturošs alkīnu analogs ( Amerikas Ķīmijas biedrības žurnāls, 2005, 127, 12232–12233, doi: 10.1021/ja053247a). Šis process, kas var šķist parasts, ir interesants divu iemeslu dēļ. Pirmkārt, neskatoties uz analoģiju alkīnu un dīgļu struktūrā, ūdeņradis reaģē ar pēdējiem nevis saskaņā ar scenāriju, kas raksturīgs ogļūdeņražiem ar oglekļa-oglekļa trīskāršo saiti (ūdeņradis pievienojas katram no trīskāršās saites atomiem, un dīglis pārvēršas par germene), bet saskaņā ar pārejas metālu atomiem raksturīgu mehānismu. Šo mehānismu, kā rezultātā elementam pievienojas ūdeņraža molekula un veidojas divas jaunas E-H saites (aprakstītajā gadījumā Ge-H), sauc par oksidatīvo pievienošanu un ir galvenais posms daudzos katalītiskos procesos, kuros iesaistīti pārejas metāli. Otrkārt, lai gan H2 var šķist vienkāršākā un nesarežģītākā molekula, ķīmiskā saite tajā ir spēcīgākā no visām, kas var rasties starp diviem identiskiem elementiem, tāpēc šīs saites pārraušana un attiecīgi ūdeņraža aktivizēšanās katalītiskās hidrogenēšanas procesos. tas nebūt nav vienkāršs uzdevums no ķīmiskās tehnoloģijas viedokļa.
Vai ir iespējams akceptoru padarīt par donoru?
Lai elementam tiktu veikta oksidatīvā ūdeņraža pievienošana (neatkarīgi no tā, kur tas atrodas periodiskajā tabulā), tam ir jābūt noteiktām elektroniskās struktūras iezīmēm. Process E + H 2 = H-E-H notiks tikai tad, ja elements ir koordinatīvi nepiesātināts un tā brīvā orbitāle var pieņemt molekulārā ūdeņraža elektronus. Turklāt šīs brīvās orbitāles enerģijai jābūt tuvu ūdeņraža molekulārās orbitāles enerģijai, kas satur elektronus. Progress homogēno metālu kompleksu katalīzes jomā galvenokārt skaidrojams ar to, ka ķīmiķi, mainot ar metālu saistīto ligandu struktūru, var mainīt tā orbitāļu enerģiju un tādējādi tās “pielāgot” stingri noteiktām vielām, kas piedalās reakcijā. . Ilgu laiku tika uzskatīts, ka tik maiga orbitāļu enerģijas regulēšana ir iespējama tikai d-elementi, tomēr pēdējā desmitgadē izrādījās, ka priekš lpp- arī elementi. Pētnieki vislielākās cerības saista ar slāpekli saturošiem kompleksiem, kuros ligandi, tāpat kā spīles, satver koordinācijas centru (tos sauc par helātu veidojošiem ligandiem, no latīņu valodas c Hela, nags), kā arī ar salīdzinoši jaunu ligandu klasi - N-heterocikliskie karbēni.

Veiksmīgs piemērs pēdējam ir Gaja Bertrāna no Kalifornijas Universitātes Sandjego darbs, kurā šie ligandi stabilizē bora atomu ( Zinātne, 2011, 33, 6042, 610–613, doi: 10.1126/science.1207573). Parasti bora atvasinājumi, kuru ārējā slānī ir tikai trīs elektroni, darbojas kā klasisks elektronu akceptors (Lūisa skābe). Fakts ir tāds, ka boram ir nepieciešami vēl pieci elektroni, lai sasniegtu stabilu astoņu elektronu apvalku, tāpēc tas var izveidot trīs kovalentās saites no trim saviem un trīs trešās puses elektroniem, bet tam ir jāiegūst vēl divi elektroni, pieņemot kāda cita elektronu. savienojas pārī tās tukšajās elektronu šūnās. Tomēr N-heterocikliskie karbēni ir tik spēcīgi elektronu donori, ka ar tiem saistītais bors pārstāj būt akceptors – tas kļūst tik "elektroniem bagāts", ka pārvēršas no Lūisa skābes par Lūisa bāzi. Vēl nesen ķīmiķi pat nevarēja paredzēt tik būtiskas izmaiņas labi zināmā īpašībās lpp- elements. Un, lai gan Bertrāna darbs joprojām ir interesants tikai no teorētiskā viedokļa, pāreja no teorijas uz praksi mūsdienās notiek diezgan ātri.
Cik tālu ir līdz katalīzei?
Tātad nesen sintezētie galveno apakšgrupu elementu atvasinājumi var iesaistīties galvenajās reakcijās, kas katalizē pārejas metālu kompleksus. Diemžēl pat iepriekš minētā molekulārā ūdeņraža oksidatīvā pievienošana silīcija vai bora atomam ir tikai pirmais solis reakciju secībā, kas jāizstrādā pilnīgam katalītiskajam ciklam. Piemēram, ja mēs runājam par hidrogenēšanu galveno apakšgrupu savienojumu klātbūtnē, kuru mehānisms atveido ūdeņraža pievienošanas mehānismu Vilkinsona katalizatora klātbūtnē, tad pēc mijiedarbības ar ūdeņradi. lpp-elementam ir jāveido komplekss ar alkēnu, tad jānotiek hidrīda pārnesei un kompleksai... un visas pārējās darbības, kas galu galā novedīs pie galaprodukta veidošanās un katalītiski aktīvo sugu reģenerācijas. Tikai tad viena katalizatora daļiņa radīs desmitiem, simtiem vai pat tūkstošiem mērķa produkta molekulu. Bet, lai šāds katalītiskais cikls darbotos, jāatrisina vēl daudzas problēmas - oksidatīvās pievienošanas rezultātā izveidotā elementa-ūdeņraža saite nedrīkst būt pārāk spēcīga (pretējā gadījumā hidrīda pārnešana nenotiks), elements, kas ir pievienojis ūdeņradim ir jāsaglabā zems koordinācijas stāvoklis, lai mijiedarbotos ar alkēnu un tā tālāk. Ja kādu brīdi palaidīsit garām, katalizators pazudīs lpp-elements nedarbosies, neskatoties uz tā uzvedības līdzību ar d-elementi dažos procesos.
Var šķist, ka pāreja no metālu kompleksa katalīzes uz katalīzi ar galveno apakšgrupu elementu savienojumiem ir pārāk grūts uzdevums, un tas ir ļoti tālu no pabeigšanas. Tomēr interese par ķīmiju lpp-elementi un sintētisko ķīmiķu vēlme platīna vai pallādija katalizatorus aizstāt ar kaut ko citu noteikti nodrošinās izrāvienu šajā virzienā. Pastāv iespēja, ka tuvākās desmitgades laikā mēs dzirdēsim par katalizatoriem, kuru pamatā ir galveno apakšgrupu koordinatīvi nepiesātinātie elementi.
2011. gada sākumā IUPAC atzina JINR sadarbību ar LLNL (ASV) par prioritāti 114. un 116. elementu atklāšanā, kas tika nosaukti: elements 114 - Flerovium, Fl; 116 elements ― Livermorium, Lv.
Flerovijs - par godu nosauktajai Kodolreakciju laboratorijai. G. N. Flerovs JINR, kas ir atzīts līderis supersmago elementu sintēzes jomā, un tā dibinātājs, izcilais fiziķis akadēmiķis G. N. Flerovs (1913–1990) - jauna veida spontānas dalīšanās radioaktivitātes autors. nuclei, vairāku jaunu zinātnes virzienu dibinātājs, FLNR JINR dibinātājs un pirmais direktors, kas tagad nes viņa vārdu.
Livermorium - par godu Livermoras Nacionālajai laboratorijai. Lorenss un tās atrašanās vieta – Livermoras pilsēta (Kalifornija, ASV). Livermoras zinātnieki vairāk nekā 20 gadus piedalās jaunu elementu sintēzes eksperimentos, kas veikti Dubnā.
Kopumā IUPAC lēmums ir atzinība par JINR zinātnieku izcilo ieguldījumu supersmago elementu “stabilitātes salas” atklāšanā, kas ir viens no svarīgākajiem mūsdienu kodolfizikas sasniegumiem.