|
초중원소의 원자핵 존재에도 제한이 있습니다. Z > 92인 원소는 자연 조건에서 발견되지 않았습니다. 액체 방울 모델을 사용한 계산은 Z2/A ≒ 46(대략 요소 112)인 핵에 대한 핵분열 장벽의 소멸을 예측합니다. 초중핵 합성 문제에서는 두 가지 쟁점이 구분되어야 한다.
- 초중핵은 어떤 특성을 가져야 합니까? 이 Z와 N 영역에 마법의 숫자가 있을까요? 초중핵의 주요 붕괴 채널과 반감기는 무엇입니까?
- 초중핵, 충격 핵의 유형, 예상 단면적 값, 예상되는 화합물 핵의 여기 에너지 및 탈여기 채널을 합성하려면 어떤 반응을 사용해야 합니까?
초중핵의 형성은 표적 핵과 입사 입자의 완전한 융합의 결과로 발생하기 때문에 충돌하는 두 핵이 복합 핵으로 융합되는 과정의 역학을 설명하는 이론적 모델을 만드는 것이 필요합니다.
초중원소 합성 문제는 Z,N = 8, 20, 28, 50, 82, N = 126(마법수)인 핵이 다양한 방사성 붕괴 방식에 대해 안정성이 증가한다는 사실과 밀접한 관련이 있습니다. 이 현상은 쉘 모델의 프레임워크 내에서 설명됩니다. 매직 넘버는 채워진 쉘에 해당합니다. 당연히 Z와 N에 다음과 같은 마법의 숫자가 존재하는지에 대한 의문이 제기됩니다. N > 150, Z > 101인 원자핵의 N-Z 다이어그램 영역에 마법 숫자가 존재한다면 초중핵은 반감기가 증가하여 관찰되어야 합니다. 즉. 안정의 섬이 있어야 합니다. 이번 연구에서는 스핀-궤도 상호작용을 고려한 우즈-색슨 전위를 이용해 수행한 계산을 바탕으로 Z=114인 핵, 즉 다음 핵의 경우 핵의 안정성이 증가할 것으로 예상되는 것으로 나타났다. 채워진 양성자 껍질은 Z = 114에 해당하고, 채워진 중성자 껍질은 숫자 N에 해당합니다. ~
184. 닫힌 껍질은 핵분열 장벽의 높이를 크게 증가시켜 핵의 수명을 늘릴 수 있습니다. 따라서 이 핵 영역(Z = 114, N ~
184) 안정의 섬을 찾아야 합니다. 작업에서도 동일한 결과가 독립적으로 얻어졌습니다.
Z = 101–109인 핵은 1986년 이전에 발견되었으며 다음과 같이 명명되었습니다: 101 - Md(Menelevium), 102 - No(Nobelium), 103 - Lr(Lawrencium), 104 - Rf(Rutherfordium, 106 - Sg(Seaborgium), 107 - Ns(Nielsborium), 108 - Hs(Hassium), 109 - Mt(Meitnerium) 1997년에 수많은 중원소 동위원소(102-105)를 발견한 Dubna 연구자들의 장점을 고려하여, 순수응용화학 총회 결정에 따라 Z = 105인 원소에 Dubnium(Db)이라는 이름이 지정되었습니다. 이 원소는 이전에 Ha(Hannium)라고 불렸습니다.

쌀. 12.3. 동위원소 Ds(Z = 110), Rg(Z = 111), Cn(Z = 112)의 붕괴 사슬.
초중핵 연구의 새로운 단계는 등록 효율성이 크게 향상되고 초중핵을 관찰하는 기술이 개선된 1994년에 시작되었습니다. 그 결과 동위원소 Ds(Z=110), Rg(Z=111), Cn(Z=112)이 발견됐다.
초중핵을 얻기 위해 50 Ti, 51 V, 58 Fe, 62 Ni, 64 Ni, 70 Zn 및 82 Se의 가속 빔이 사용되었습니다. 동위원소 208 Pb 및 209 Bi가 표적으로 사용되었습니다. 110번 원소의 다양한 동위원소는 그 이름을 딴 핵반응연구소에서 합성되었습니다. G.N. 반응 244 Pu(34 S,5n) 272 110을 사용하고 GSI(Darmstadt)에서 반응 208 Pb(62 Ni,n) 269 110을 사용하는 Flerov. 동위원소 269 Ds, 271 Ds, 272 Rg 및 277 Cn은 다음과 같이 기록되었습니다. 붕괴 사슬에 연결됩니다(그림 12.3).
초중원소 생산에서 중요한 역할은 화학원소의 예상 특성과 화학원소가 형성될 수 있는 반응을 계산하는 이론적 모델에 의해 수행됩니다.
다양한 이론적 모델을 바탕으로 초중핵의 붕괴 특성을 계산했습니다. 그러한 계산의 결과가 그림 1에 나와 있습니다. 12.4. 짝수-짝수 초중핵의 반감기는 자발적 핵분열(a), α-붕괴(b), β-붕괴(c) 및 가능한 모든 붕괴 과정(d)에 대해 제공됩니다. 자연분열과 관련하여 가장 안정적인 핵(그림 12.4a)은 Z = 114이고 N = 184인 핵입니다. 이 경우 자연분열과 관련된 반감기는 ~10 16 년입니다. 가장 안정한 동위원소와 6~8개의 중성자가 다른 114번 원소의 동위원소의 경우 반감기는
10~15배 정도. α-붕괴에 대한 반감기는 그림 1에 나와 있습니다. 12.5b. 가장 안정적인 코어는 Z = 114 및 N = 184(T 1/2 = 10 15년) 영역에 위치합니다.
β-붕괴에 대해 안정한 핵은 그림 1에 나와 있습니다. 12.4v에 검은 점이 있습니다. 그림에서. 그림 12.4d는 중앙 윤곽선 내부에 위치한 짝수-짝수 핵의 총 반감기가 ~10 5 년임을 보여줍니다. 따라서 모든 유형의 붕괴를 고려한 결과 Z = 110 및 N = 184 근처의 핵이 "안정성의 섬"을 형성하는 것으로 나타났습니다. 294 110 핵의 반감기는 약 10 9 년입니다. 쉘 모델에 의해 예측된 Z 값과 매직 넘버 114의 차이는 핵분열(Z = 114인 핵이 가장 안정적인 핵)과 α-붕괴(Z가 낮은 핵이 안정적인 핵) 간의 경쟁으로 인해 발생합니다. ). 홀짝수 핵과 짝수홀수 핵은 상대적으로 반감기가 있습니다.
α-붕괴와 자연분열은 증가하고, β-붕괴와 관련하여 감소합니다. 위의 추정치는 계산에 사용된 매개변수에 크게 의존하며 실험적 탐지에 충분한 수명을 가진 초중핵의 존재 가능성을 나타내는 지표로만 간주될 수 있다는 점에 유의해야 합니다.

쌀. 12.4. 짝수 초중핵에 대해 계산된 반감기(숫자는 반감기를 연 단위로 나타냄):
a - 자연 핵분열 관련, b - α-붕괴, c - e-포획 및 β-붕괴, d - 모든 붕괴 과정에 대해
초중핵의 평형 형태와 반감기에 대한 또 다른 계산 결과가 그림 1에 나와 있습니다. 12.5, 12.6. 그림에서. 그림 12.5는 Z = 104-120인 핵의 중성자와 양성자 수에 대한 평형 변형 에너지의 의존성을 보여줍니다. 변형 에너지는 평형 상태와 구형 상태의 핵 에너지 간의 차이로 정의됩니다. 이 데이터로부터 Z = 114 및 N = 184 영역에는 바닥 상태에서 구형 모양을 갖는 핵이 있어야 한다는 것이 분명합니다. 현재까지 발견된 모든 초중핵(그림 12.5에 어두운 다이아몬드로 표시됨)은 변형되었습니다. 밝은 다이아몬드는 β-붕괴에 대해 안정적인 핵을 보여줍니다. 이들 핵은 α 붕괴 또는 핵분열에 의해 붕괴되어야 합니다. 주요 붕괴 채널은 α-붕괴여야 합니다.
짝수-짝수 β-안정 동위원소의 반감기는 그림 1에 나와 있습니다. 12.6. 이러한 예측에 따르면 대부분의 핵의 반감기는 이미 발견된 초중핵(0.1~1ms)에서 관찰된 것보다 훨씬 더 길 것으로 예상됩니다. 예를 들어, 292 Ds 핵의 경우 수명은 ~51년으로 예측됩니다.
따라서 현대 현미경 계산에 따르면 초중핵의 안정성은 중성자 마법수 N = 184에 가까워질수록 급격히 증가합니다. 최근까지 Z = 112 Cn(코페르니슘) 원소의 유일한 동위원소는 동위원소 277 Cn이었습니다. 반감기는 0.24ms입니다. 더 무거운 동위원소인 283 Cn은 저온 핵융합 반응인 48 Ca + 238 U에서 합성되었습니다. 조사 시간은 25일이었습니다. 타겟에 있는 총 48개의 Ca 이온 수는 3.5·10 18 입니다. 생성된 동위원소 283 Cn의 자발적인 핵분열로 해석되는 두 가지 사례가 기록되었습니다. 이 새로운 동위원소의 예상 반감기는 T 1/2 = 81초입니다. 따라서 277 Cn 동위원소에 비해 283 Cn 동위원소의 중성자 수가 6 단위 증가하면 수명이 5배 정도 증가한다는 것이 분명합니다.
그림에서. 12.7 연구에서 가져온 실험적으로 측정된 α-붕괴 기간은 핵의 껍질 구조를 고려하지 않고 액체 방울 모델을 기반으로 한 이론적 계산 결과와 비교됩니다. 우라늄의 가벼운 동위원소를 제외하고 모든 중핵의 경우 껍질 효과로 인해 대부분의 핵에서 반감기가 2~5배 증가한다는 것을 알 수 있습니다. 핵의 껍질 구조는 상대적으로 자발적인 핵분열의 반감기에 훨씬 더 큰 영향을 미칩니다. Pu 동위원소의 반감기 증가는 몇 자릿수이며 260 Sg 동위원소의 경우 증가합니다.
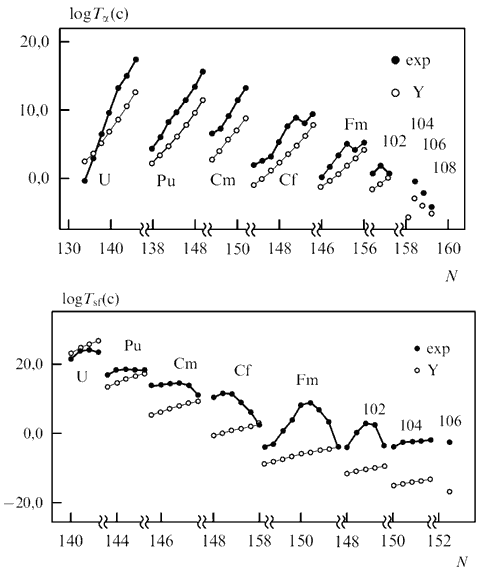
쌀. 12.7. 핵의 껍질 구조를 고려하지 않고 액체 방울 모델을 기반으로 한 초우라늄 원소의 실험적으로 측정된(● exp) 및 이론적으로 계산된(○ Y) 반감기. 위쪽 그림은 α 붕괴의 반감기이고, 아래쪽 그림은 자연분열의 반감기입니다. 그림에서. 그림 12.8은 다양한 이론적 모델의 예측과 비교하여 시보듐 동위원소 Sg(Z = 106)의 측정된 수명을 보여줍니다. 주목할 만한 점은 N = 164인 동위원소의 수명이 N = 162인 동위원소의 수명에 비해 거의 10배 정도 감소한다는 것입니다.
안정도에 가장 가까운 접근은 76 Ge + 208 Pb 반응에서 달성될 수 있습니다. 초중비 거의 구형 핵은 핵융합 반응에 이어 γ 양자 또는 단일 중성자가 방출되면서 형성될 수 있습니다. 추정에 따르면, 생성된 284 114 핵은 반감기가 ~ 1 ms인 α 입자의 방출과 함께 붕괴되어야 합니다. N = 162 영역에서 껍질의 점유에 대한 추가 정보는 271 Hs 및 267 Sg 핵의 α 붕괴를 연구하여 얻을 수 있습니다. 이 핵의 반감기는 1분으로 예상됩니다. 그리고 1시간. 핵 263 Sg, 262 Bh, 205 Hs, 271,273 Ds의 경우 이성질체의 발현이 예상되며 그 이유는 핵의 경우 N = 162 영역에서 j = 1/2 및 j = 13/2로 하위 껍질을 채우기 때문입니다. 바닥 상태에서 변형되었습니다.
그림에서. 그림 12.9는 입사 이온 50 Ti 및 56 Fe와 타겟 핵 208 Pb의 융합 반응을 위한 원소 Rf(Z = 104) 및 Hs(Z = 108) 형성 반응에 대해 실험적으로 측정된 여기 함수를 보여줍니다.
생성된 복합핵은 하나 또는 두 개의 중성자를 방출하여 냉각됩니다. 중이온 융합 반응의 여기 기능에 대한 정보는 초중핵을 얻는 데 특히 중요합니다. 중이온의 핵융합 반응에서는 쿨롱력과 표면장력의 영향을 정확하게 균형잡는 것이 필요합니다. 입사 이온의 에너지가 충분히 높지 않으면 최소 접근 거리는 쌍성 핵 시스템의 병합에 충분하지 않습니다. 입사 입자의 에너지가 너무 높으면 결과 시스템은 높은 여기 에너지를 가지며 조각으로 분해될 가능성이 높습니다. 효과적인 융합은 충돌하는 입자의 다소 좁은 에너지 범위에서 발생합니다.

그림 12.10. 64 Ni와 208 Pb의 융합 가능성 다이어그램.
최소한의 중성자 수(1~2)를 방출하는 핵융합 반응이 특히 중요합니다. 합성된 초중핵에서는 가능한 가장 큰 N/Z 비율을 갖는 것이 바람직합니다. 그림에서. 그림 12.10은 64 Ni + 208 Pb → 272 Ds 반응에서 핵의 융합 가능성을 보여줍니다. 가장 간단한 추정치는 핵융합에 대한 터널 효과의 확률이 ~10-21이며 이는 관측된 단면 값보다 상당히 낮다는 것을 보여줍니다. 이는 다음과 같이 설명될 수 있습니다. 핵 중심 사이의 14fm 거리에서 236.2MeV의 초기 운동 에너지는 쿨롱 전위에 의해 완전히 보상됩니다. 이 거리에서는 핵 표면에 위치한 핵만 접촉합니다. 이 핵자의 에너지는 낮습니다. 따라서 핵자 또는 핵자 쌍이 한 핵의 궤도를 떠나 파트너 핵의 자유 상태로 이동할 확률이 높습니다. 입사 핵에서 표적 핵으로의 핵 이동은 납 208 Pb의 이중 마법 동위원소가 표적으로 사용되는 경우 특히 매력적입니다. 208 Pb에서는 양성자 하위 껍질 h 11/2와 중성자 하위 껍질 h 9/2 및 i 13/2가 채워져 있습니다. 처음에 양성자 이동은 양성자-양성자 인력에 의해 자극되고, h 9/2 서브쉘을 채운 후에는 양성자-중성자 인력에 의해 자극됩니다. 마찬가지로, 중성자는 이미 채워진 하위 껍질 i 13/2의 중성자에 이끌려 자유 하위 껍질 i 11/2로 이동합니다. 짝짓기 에너지와 큰 궤도 각모멘트로 인해 한 쌍의 핵자 이동이 단일 핵자 이동보다 더 가능성이 높습니다. 64 Ni 208 Pb에서 두 개의 양성자가 이동한 후 쿨롱 장벽은 14 MeV만큼 감소하여 상호 작용하는 이온의 더 가까운 접촉과 핵자 이동 과정의 지속을 촉진합니다.
[V.V. 볼코프. 깊은 비탄성 전달의 핵 반응. M. Energoizdat, 1982; V.V. 볼코프. Izv. 소련 과학 아카데미, 물리적 시리즈, 1986, vol. 1879] 핵융합 반응의 메커니즘이 자세히 연구되었습니다. 이미 포획 단계에서 입사 입자의 운동 에너지가 완전히 소멸된 후 이중 핵 시스템이 형성되고 핵 중 하나의 핵이 점차적으로 껍질별로 다른 핵으로 전달되는 것으로 나타났습니다. 즉, 핵의 껍질 구조가 복합핵의 형성에 중요한 역할을 한다는 것이다. 이 모델을 기반으로, 복합 핵의 여기 에너지와 저온 핵융합 반응에서 원소 Z = 102-112의 형성에 대한 단면을 아주 잘 설명하는 것이 가능했습니다.
따라서 초우라늄 원소 Z = 107-112 합성의 진전은 마법 동위원소 208 Pb 및 209 Bi에 Z = 22-30인 이온이 조사되는 저온 핵융합 반응의 "발견"과 관련이 있습니다. 상온 핵융합 반응에서 형성된 핵은 중성자 1개의 방출로 인해 약하게 가열되고 냉각됩니다. 이것이 Z = 107-112인 화학 원소의 동위원소가 처음으로 얻은 방법입니다. 이 화학 원소는 1978~1998년에 획득되었습니다. 독일 다름슈타트의 GSI 연구 센터에 특별히 제작된 가속기입니다. 그러나 이 방법을 사용하여 더 무거운 핵으로 더 나아가는 것은 충돌하는 핵 사이의 잠재적 장벽이 증가하기 때문에 어려운 것으로 밝혀졌습니다. 따라서 초중핵을 생성하는 또 다른 방법이 Dubna에서 구현되었습니다. 인공적으로 얻은 화학 원소인 플루토늄 Pu(Z = 94), 아메리슘 Am(Z = 95), 큐륨 Cm(Z = 96), 베르켈륨 Bk(Z = 97) 및 칼리포르늄 Cf(Z = 98) 중 가장 무거운 동위원소가 사용되었습니다. 목표로. 칼슘 동위원소 48 Ca(Z = 20)가 가속 이온으로 선택되었습니다. 반동 핵 분리기 및 검출기의 개략도가 그림 1에 나와 있습니다. 12.11.
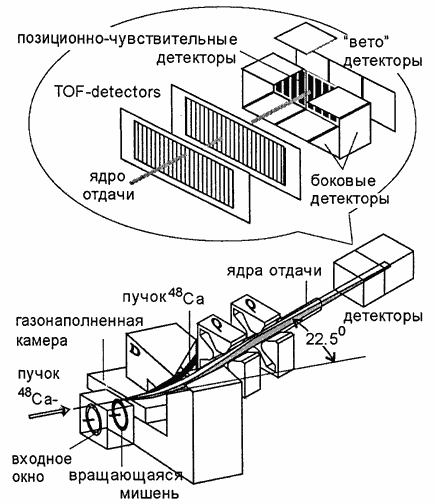
쌀. 12.11. Dubna에서 초중원소 합성 실험이 수행되는 반동 핵 분리기의 개략도.
반동 핵의 자기 분리기는 반응 부산물의 배경을 10 5 –10 7 배 감소시킵니다. 반응 생성물은 위치 감지 실리콘 검출기를 사용하여 기록되었습니다. 반동 핵의 에너지, 좌표 및 비행 시간이 측정되었습니다. 정지 후, 감지된 붕괴 입자의 모든 후속 신호는 이식된 핵의 정지 지점에서 나와야 합니다. 생성된 기술을 통해 검출기에 정지된 초중핵과 그 붕괴 생성물 사이의 연결을 높은 수준의 신뢰성(약 100%)으로 설정할 수 있었습니다. 이 기술을 사용하면 초중량 요소는 다음과 같습니다.
Z = 110–118(표 12.2)
표 12.2는 Z = 110–118인 초중화학 원소의 특성을 보여줍니다. 질량수 A, m - 질량수 A, 스핀 패리티 JP, 핵 결합 에너지 Est, 특정 결합 에너지 ε를 갖는 동위원소에 이성질체 상태의 존재, 중성자 분리 에너지 B n 및 양성자 B p , 반감기 T 1/2 및 주요 붕괴 채널.
화학 원소 Z > 112에는 아직 이름이 없으며 허용되는 국제 표기법으로 제공됩니다.
표 12.2
초중화학원소의 특성 Z = 110–118
| 오전 XX시 |
JP |
무게
커널,
MeV |
E 스트리트,
MeV |
ε,
MeV |
비엔,
MeV |
BP,
MeV |
티 1/2 |
감쇠 모드 |
|---|
| Z = 110 − 다름스타튬 |
|---|
| DS-267 |
|
248787.19
|
1934.5
|
7.2
|
|
0.7
|
2.8AC |
α ≒100% |
| DS-268 |
0 +
|
249718.08
|
1943.2
|
7.3
|
8.7
|
1.3
|
100AC |
α
≈
|
| DS-269 |
|
250650.86
|
1950.0
|
7.2
|
6.8
|
1.3
|
179AC |
α 100% |
| DS-270 |
0 +
|
251581.97
|
1958.4
|
7.3
|
8.5
|
|
0.10ms |
α 100%, SF< 0.20%
|
| DS-270-m |
|
251583.07
|
1957.3
|
7.2
|
|
|
6.0ms |
α >70%, IT ≤ 30% |
| Ds-271 |
|
252514.72
|
1965.2
|
7.3
|
6.8
|
2.2
|
1.63ms |
α ≒100% |
| Ds-271-m |
|
252514.72
|
1965.2
|
7.3
|
|
|
69ms |
IT?, α >0% |
| Ds-272 |
0 +
|
253446.46
|
1973.1
|
7.3
|
7.8
|
2.5
|
1초 |
SF |
| Ds-273 |
|
254380.32
|
1978.8
|
7.2
|
5.7
|
2.5
|
0.17ms |
α ≒100% |
| DS-274 |
0 +
|
255312.45
|
1986.2
|
7.2
|
7.4
|
3.0
|
2초 |
α?,
SF? |
| Ds-275 |
|
256246.44
|
1991.8
|
7.2
|
5.6
|
2.9
|
2초 |
α?
|
| DS-276 |
0 +
|
257178.73
|
1999.1
|
7.2
|
7.3
|
3.2
|
5초 |
SF?,
α?
|
| Ds-277 |
|
258112.63
|
2004.7
|
7.2
|
5.7
|
3.1
|
5초 |
α?
|
| DS-278 |
0 +
|
259044.92
|
2012.0
|
7.2
|
7.3
|
|
10초 |
SF?,
α?
|
| Ds-279 |
|
259978.62
|
2017.9
|
7.2
|
5.9
|
|
0.18초 |
SF ≒90%,
α ≒10% |
| Ds-281 |
|
261844.60
|
2031.0
|
7.2
|
|
|
9.6초 |
SF 100% |
| Z =111 − 뢴트게늄 |
|---|
| Rg-272 |
|
253452.75
|
1965.5
|
7.2
|
|
0.2
|
3.8ms |
α ≒100% |
| Rg-273 |
|
254384.34
|
1973.5
|
7.2
|
8.0
|
0.4
|
5ms |
α?
|
| Rg-274 |
|
255317.74
|
1979.6
|
7.2
|
6.2
|
0.9
|
6.4ms |
α ≒100% |
| Rg-275 |
|
256249.53
|
1987.4
|
7.2
|
7.8
|
1.2
|
10ms |
α?
|
| Rg-276 |
|
257183.22
|
1993.3
|
7.2
|
5.9
|
1.5
|
100ms |
SF?,
α?
|
| Rg-277 |
|
258115.72
|
2000.4
|
7.2
|
7.1
|
1.3
|
1초 |
α?,
SF? |
| Rg-278 |
|
259049.11
|
2006.5
|
7.2
|
6.2
|
1.8
|
4.2ms |
α 100%,
SF |
| Rg-279 |
|
259981.41
|
2013.8
|
7.2
|
7.3
|
1.8
|
0.17초 |
α ≒100% |
| Rg-280 |
|
260914.80
|
2020.0
|
7.2
|
6.2
|
2.1
|
3.6초 |
α ≒100% |
| Rg-281 |
|
261847.09
|
2027.2
|
7.2
|
7.3
|
|
1m |
α?, SF? |
| Rg-282 |
|
262780.59
|
2033.3
|
7.2
|
6.1
|
2.3
|
4m |
SF?, α? |
| Rg-283 |
|
263712.98
|
2040.5
|
7.2
|
7.2
|
|
10m |
SF?, α? |
| Z = 112 − 코페르니슘 |
|---|
| Cn-277 |
|
258119.32
|
1995.5
|
7.2
|
|
2.2
|
0.69ms |
α ≒100% |
| Cn-278 |
0 +
|
259051.20
|
2003.1
|
7.2
|
7.7
|
2.8
|
10ms |
SF?, α? |
| Cn -279 |
|
259984.69
|
2009.2
|
7.2
|
6.1
|
2.7
|
0.1초 |
SF?, α? |
| Cn -280 |
0 +
|
260916.69
|
2016.8
|
7.2
|
7.6
|
3.0
|
1초 |
α?, SF? |
| Cn-282 |
0 +
|
262782.18
|
2030.4
|
7.2
|
|
3.2
|
0.50ms |
SF 100% |
| Cn-283 |
|
263715.57
|
2036.6
|
7.2
|
6.2
|
3.3
|
4.0초 |
α ≥90%, SF ≤10% |
| Cn-284 |
0 +
|
264647.66
|
2044.1
|
7.2
|
7.5
|
3.6
|
101ms |
SF 100% |
| Cn -285 |
|
265580.76
|
2050.5
|
7.2
|
6.5
|
|
34초 |
α ≒100% |
| Z=113 |
|---|
| Uut-278 |
|
|
|
|
|
|
0.24ms |
α 100% |
| Uut-283 |
|
263719.46
|
2031.4
|
7.2
|
|
1.0
|
100ms |
α 100% |
| Uut-284 |
|
264652.45
|
2038.0
|
7.2
|
6.6
|
1.4
|
0.48초 |
α ≒100% |
| Uut-285 |
|
265584.55
|
2045.5
|
7.2
|
7.5
|
1.4
|
2m |
α?, SF? |
| Uut-286 |
|
266517.64
|
2051.9
|
7.2
|
6.5
|
1.4
|
5m |
α?, SF? |
| Uut-287 |
|
267449.64
|
2059.5
|
7.2
|
7.6
|
|
20m |
α?, SF? |
| Z=114 |
|---|
| 우크-286 |
0 +
|
266520.33
|
2048.0
|
7.2
|
|
2.5
|
0.16초 |
SF ≒60%, α ≒40% |
| 우크-287 |
|
267453.42
|
2054.4
|
7.2
|
6.5
|
2.5
|
0.51초 |
α ≒100% |
| 우크-288 |
0 +
|
268385.02
|
2062.4
|
7.2
|
8.0
|
2.9
|
0.80초 |
α ≒100% |
| 우크-289 |
|
269317.91
|
2069.1
|
7.2
|
6.7
|
|
2.7초 |
α ≒100% |
| Z=115 |
|---|
| 업-287 |
|
267458.11
|
2048.4
|
7.1
|
|
0.5
|
32ms |
α 100% |
| 업-288 |
|
268390.81
|
2055.3
|
7.1
|
6.9
|
0.9
|
87ms |
α 100% |
| 업-289 |
|
269322.50
|
2063.2
|
7.1
|
7.9
|
0.8
|
10초 |
SF?, α? |
| 업-290 |
|
270255.30
|
2070.0
|
7.1
|
6.8
|
0.9
|
10초 |
SF?, α? |
| 업-291 |
|
271187.09
|
2077.7
|
7.1
|
7.8
|
|
1m |
α?, SF? |
| Z=116 |
|---|
| 으어-290 |
0 +
|
270258.98
|
2065.0
|
7.1
|
|
1.8
|
15ms |
α ≒100% |
| 으어-291 |
|
271191.78
|
2071.7
|
7.1
|
6.8
|
1.8
|
6.3ms |
α 100% |
| 으어-292 |
0 +
|
272123.07
|
2080.0
|
7.1
|
8.3
|
2.3
|
18ms |
α ≒100% |
| 으어-293 |
|
|
|
|
|
|
53ms |
α ≒100% |
| Z=117 |
|---|
| Uus-291 |
|
271197.37
|
2064.9
|
7.1
|
|
-0.1
|
10ms |
SF?, α? |
| Uus-292 |
|
272129.76
|
2072.0
|
7.1
|
7.2
|
0.3
|
50ms |
SF?, α? |
| Z=118 |
|---|
| 우오-294 |
0 +
|
|
|
|
|
|
1.8ms |
α ≒100% |
그림에서. 그림 12.12는 합성 반응에서 얻은 Z = 110-118인 알려진 가장 무거운 동위원소를 모두 보여주며, 이는 실험적으로 측정된 반감기를 나타냅니다. 안정성 섬의 이론적으로 예측된 위치도 여기에 표시됩니다(Z = 114, N = 184).

쌀. 12.12. 요소 Z = 110–118의 N-Z 다이어그램.
얻은 결과는 이중 마법핵(Z = 114, N = 184)에 접근함에 따라 동위원소의 안정성이 증가한다는 것을 분명히 나타냅니다. Z = 110 및 112인 핵에 7~8개의 중성자를 추가하면 반감기가 2.8(Ds-267)에서 10s(Ds-168, Ds 271)로 증가합니다. 반감기는 T 1/2(272 Rg, 273 Rg) ≒ 4–5 ms가 T 1/2(283 Rg) ≒ 10분으로 증가합니다. Z = 110–112 원소의 가장 무거운 동위원소에는 170개의 중성자가 포함되어 있으며 이는 여전히 마법수 N = 184와는 거리가 멀습니다. 결과적으로 Z > 111 및 N > 172인 가장 무거운 동위원소는 모두 주로 붕괴됩니다.
α-붕괴, 자발적 핵분열 - 더 드물게 붕괴됩니다. 이러한 결과는 이론적 예측과 잘 일치합니다.
이름을 딴 핵반응연구소에서. G.N. Flerov(Dubna)는 Z = 114인 원소를 합성했습니다. 반응식을 사용했습니다.
289 114 핵의 식별은 일련의 α 붕괴를 사용하여 수행되었습니다. 동위원소의 반감기에 대한 실험적 평가 289 114 ~30초. 얻은 결과는 이전에 수행한 계산과 잘 일치합니다.
반응 48 Cu + 244 Pu에서 원소 114를 합성하는 동안 Z = 114인 동위원소의 최대 수율이 3개의 중성자가 증발하는 채널에서 관찰되었습니다. 이 경우, 복합핵(289,114)의 여기 에너지는 35MeV였다.
248 Cm + 48 Ca → 296 116 반응에서 형성된 296 116 핵에서 발생하는 이론적으로 예측된 일련의 붕괴가 그림 12.13에 나와 있습니다.

쌀. 12.13. 핵 붕괴 다이어그램 296 116.
동위원소 296 116은 4개의 중성자 방출의 결과로 냉각되어 동위원소 292 116으로 변합니다. 그런 다음 5% 확률로 두 번의 연속 e-포획의 결과로 동위원소 292 114로 변합니다. 결과적으로 α 붕괴(T 1/2 = 85일) 동위원소 292 114가 동위원소 288 112로 변합니다. 동위원소 288 112의 형성도 채널을 통해 발생합니다.
두 사슬에서 생성된 최종 핵 288 112 은 약 1시간의 반감기를 갖고 자발적인 핵분열에 의해 붕괴됩니다. 대략 10%의 확률로 동위원소 288(114)의 α-붕괴의 결과로 동위원소(284)(112)가 형성될 수 있습니다. 위의 주기와 붕괴 채널은 계산에 의해 얻어졌습니다.
그림에서. 그림 12.14는 Dubna의 실험에서 측정된 동위원소 288115의 일련의 연속적인 α-붕괴를 보여줍니다. ER은 위치 감지 실리콘 탐지기에 이식된 반동 핵의 에너지입니다. 세 가지 실험에서 α-붕괴의 반감기와 에너지가 잘 일치한다는 것을 알 수 있는데, 이는 α 입자의 스펙트럼 측정을 사용하여 초중원소를 식별하는 방법의 신뢰성을 나타냅니다.

쌀. 12.14. Dubna의 실험에서 측정된 동위원소 288115의 일련의 연속적인 α-붕괴.
Z = 118인 실험실에서 생성된 가장 무거운 원소가 이 반응에서 합성되었습니다.
48 Ca + 249 Cf → 294 118 + 3n.
쿨롱 장벽 근처의 이온 에너지에서 원소 118이 형성되는 세 가지 사례가 관찰되었습니다. 294,118개의 핵이 실리콘 검출기에 이식되었으며 일련의 연속적인 α 붕괴가 관찰되었습니다. 요소 118의 형성을 위한 단면적은 ~2피코반이었습니다. 동위원소 293118의 반감기는 120ms입니다.
그림에서. 그림 12.15는 이론적으로 계산된 동위원소 293 118의 연속적인 α-붕괴 사슬과 α-붕괴의 결과로 형성된 딸핵의 반감기를 보여줍니다.

쌀. 12.15. 동위원소 293 118의 연속적인 α-붕괴의 사슬.
α-붕괴의 결과로 형성된 딸핵의 평균 수명이 제공됩니다.
중이온과의 반응으로 초중원소가 형성될 수 있는 다양한 가능성을 분석할 때 다음과 같은 상황을 고려해야 합니다.
- 양성자 수에 대한 중성자 수의 비율이 충분히 큰 핵을 생성해야 합니다. 따라서 N/Z가 큰 중이온을 입사입자로 선택해야 합니다.
- 생성된 복합핵은 낮은 여기 에너지와 작은 각운동량을 갖는 것이 필요합니다. 그렇지 않으면 핵분열 장벽의 유효 높이가 감소하기 때문입니다.
- 생성된 핵은 구형에 가까운 모양을 갖는 것이 필요합니다. 왜냐하면 약간의 변형이라도 초중핵의 급속한 분열로 이어질 것이기 때문입니다.
초중핵을 생성하는 매우 유망한 방법은 238 U + 238 U, 238 U + 248 Cm, 238 U + 249 Cf, 238 U + 254 Es와 같은 반응입니다. 그림에서. 그림 12.16은 가속된 238 U 이온을 사용하여 248 Cm, 249 Cf 및 254 Es 표적에 조사하는 동안 초우라늄 원소가 형성되는 추정 단면적을 보여줍니다. 이들 반응에서, Z > 100인 원소의 형성에 대한 단면에 대한 첫 번째 결과는 연구 중인 반응의 수율을 높이기 위해 반응 생성물이 남아 있도록 목표 두께를 선택했습니다. 목표. 조사 후 개별 화학 원소가 타겟에서 분리되었습니다. α-붕괴 생성물과 핵분열 파편은 몇 달에 걸쳐 얻은 샘플에 기록되었습니다. 가속된 우라늄 이온을 사용하여 얻은 데이터는 가벼운 충격 이온에 비해 무거운 초우라늄 원소의 수율이 증가한다는 것을 분명히 나타냅니다. 이 사실은 초중핵 융합 문제를 해결하는 데 매우 중요합니다. 적절한 목표를 설정하는 데 어려움이 있음에도 불구하고 높은 Z를 향한 진전에 대한 예측은 매우 낙관적입니다.

쌀. 12.16. 238 U와 248 Cm, 249 Cf 및 254 Es의 반응에서 초우라늄 원소 형성에 대한 단면적 추정
최근 몇 년간 초중핵 분야의 발전은 놀랄 만큼 인상적이었습니다. 그러나 안정의 섬을 발견하려는 모든 시도는 지금까지 성공하지 못했습니다. 그에 대한 수색은 집중적으로 계속되고 있습니다.
원자핵의 껍질 구조는 초중핵의 안정성을 높이는 데 중요한 역할을 합니다. 마법의 숫자 Z ≒ 114 및 N ≒ 184가 실제로 존재한다면 원자핵의 안정성이 크게 증가할 수 있습니다. α-붕괴의 결과로 초중핵의 붕괴가 일어난다는 점도 중요하며, 이는 새로운 초중핵을 검출하고 식별하기 위한 실험 방법 개발에 중요합니다.
|
화학요법의 '화학 시대'는 다음과 같은 물질의 개발로 시작되었습니다.
제조업. 뛰어난 분석
마르크스와 레닌은 그 과정이 어떻게 진행되었는지 보여줍니다.
산업계 자본주의의 발전: 단순한 협력에서
제조업을 통한 노동(16~7세기) 산업
18세기 말과 19세기 초 자본주의 체제로 전환했다.
공장, 즉 대규모 기계 생산.
육체 노동은 기계 노동으로 대체되었습니다.
증기기관, 철도 및 해상운송의 발전
증기 수송, 기계 방적, 새로운 방법
주철과 강철 - 이 모든 것이 산업 혁명을 일으켰습니다.
산업혁명 시대가 도래했습니다.
화학과학은 기계과학의 요구를 간신히 따라잡을 수 있었습니다.
산업. 이론 분야에서 이 과학은
18세기 중반에 큰 도약을 이루었습니다.
과학 화학과 열역학의 기초는 우리에 의해 마련되었습니다.
유명한 동포 Lomonosov.
1748년 러시아 과학 아카데미 회원인 수학자 오일러에게 보낸 유명한 편지에서 로모노소프는 처음으로 다음과 같은 공식을 공식화했습니다.
물질과 운동의 불변의 법칙. 그를
두 번째로 중요한 장점에 속합니다. 그는 승진했습니다.
원자 문제를 연구해야 할 필요성에 대한 아이디어
물질의 분자 구조 때문에
모든 신체의 특성, 화학적, 물리적 특성.
`` ...화학” 로모노소프는 화학의 이점에 관해 그의 말씀에서 다음과 같이 썼습니다.
첫 번째 리더는 내면을 드러내는 것입니다
시체의 전당, 내부 은신처에 가장 먼저 침투
신체, 첫 번째는 신체의 일부와 ≫에 대해 알게 될 것입니다.
`` 화학은 인간사에 손을 뻗는다
≫ - 그는 이 단어로 이 섹션 중 하나를 끝냈습니다.
〈단어〉. `` 신체의 지속적인 탄생과 파괴는 충분하다
소체의 움직임에 대해 설득력 있게 말하다》, 썼다
죽은 것, 식물에서 움직이는 것 - 살아 있는 것과 죽은 것, 광물에서
또는 무기물이므로 모든 것에서 ≫.
직조 생산의 기계화로 인해 이러한 필요성이 생겼습니다.
옥양목 인쇄 및 염색의 역학 및 화학 혁명
비즈니스, 금속 가공, 경화 필요
공정에서 화학 원소의 깊은 개입
의심할 여지 없이 현대 화학의 주요 성과는
과학은 세 명의 뛰어난 러시아 화학자 덕분에 탄생했습니다 - 니콜라이
Nikolaevich Zinin, Alexander Mikhailovich Butlerov I에게
드미트리 이바노비치 멘델레예프.
1841년 카잔 대학교 N. N. Zinin 교수
고리형 화합물로부터 화학적 합성으로 얻어짐
니트로벤젠 아닐린은 출발 제품입니다.
가공을 통해 수십 가지의 다양한 염료가 얻어집니다.
그 전에는 식물 제품으로 페인트를 준비했습니다.
Zinin은 소위 말하는 것의 아버지로 간주됩니다.
합성화학.
Zinin이 변신 외에 아무것도 하지 않았다면
니트로벤젠을 아닐린으로 바꾸면 그의 이름이 포함되었을 것입니다.
가장 위대한 화학자의 이름으로 과학의 역사. 아닐린 합성
화학, 의약산업의 새로운 시대를 열었습니다.
아닐린을 염산, 메틸알코올로 처리하여,
포스겐 및 기타 시약을 사용하면 매우
직물용 염료가 많이 있습니다. 200개 이상의 염료
소련 화학 산업에서 생산
무색 아닐린. 아닐린은 생산에 사용됩니다
필름, 컬러 필름 개발자. 아닐린에서
가황 과정을 가속화하는 물질을 생성합니다.
고무. 100개 이상의 약물 제조
현재 스트렙토사이드(streptocide)와 설폰아미드(sulfonamides)를 포함하여
아닐린의 유도체이다.
18세기에 로모노소프의 명확한 마음은 그 중요성을 예견했습니다.
의학을 위한 화학: `` 화학에 대한 충분한 지식이 없는 의사
완벽할 수는 없습니다...≫ ; `` 화학물질만으로도 희망
의학의 단점을 보완할 수 있다... 》 .
Zinin의 후계자 A.M. Butlerov는 혁명을 일으켰습니다.
유기 화합물의 구조에 관한 교리.
원자의 현실을 확신한 Butlerov는 목표를 세웠습니다.
원자 사이의 화학 결합을 정확한 공식으로 표현하고,
유기 화합물 분자를 형성합니다. 버틀레로프
분자의 구조를 알아내는 것이 가능하다고 믿었다.
물리적 방법과 화학적 변형을 통해.
이 길을 따라 그는 화학 이론을 발전시켰습니다.
유기 화합물의 구조. 끈질긴 실험 끝에
부틸 알코올을 사용하여 Butlerov는 다음 중 하나를 확립했습니다.
동일한 수의 특정 원자(예: 탄소,
수소와 산소)가 사슬로 연결되어 있고,
다양한 제품을 생산할 수 있으며 그 결과의 특성은 무엇입니까?
화학제품은 생산되는 순서에 따라 달라집니다.
요소는 서로 연결되어 있습니다. 숫자처럼 늘었어
새로운 화학 물질의 합성에서 가능한 조합,
그리고 받은 약의 개수
화학 합성에 의해.
19세기의 가장 위대한 발견은 주기율이다
멘델레예프 - . 엄격한 질서를 확립하게 되었고,
화학 원소 간의 패턴. 이것의 척도
원자량이 패턴이 되었습니다. 많은 화학요법 약물
과거에는 우연히 발견되었습니다. 그러나 과학은 무작위의 적이다.
과학적 지식이 발전하면서 신비로워 보였던 많은 것들이
이해할 수 없는 것이 명확하고 자연스러워졌습니다.
멘델레예프의 주기율은 모든 화학물질을
과학, 특히 화학요법은 확고한 과학적 기반을 바탕으로 합니다.
멘델레예프는 “주기율 이전에” 이렇게 썼습니다. 단순한
신체는 단편적이고 무작위적인 현상만을 나타냄
자연: 새로운 것을 기대할 이유가 없었지만, 또 다시
그들의 속성에서 완전히 예상치 못한 참신함이 발견되었습니다.
이를 가능하게 한 최초의 것은 주기적 합법성이었습니다.
아직 발견되지 않은 원소를 먼 거리에서 볼 수 없는 경우
이 패턴으로 무장한 케미컬 비전
모공에는 도달하지 않았으며 동시에 이전에 발견된 새로운 요소는
다양한 속성을 가지고 그려졌습니다. ≫ 1.
엥겔스가 과학적 선견지명을 특징으로 한 것은 당연합니다.
과학적 위업으로서의 멘델레예프. 정말 탁월했어요
화학 현상 과학의 승리,
인류는 해방의 항구적인 길을 택해야 한다
우연의 힘과 자연의 힘의 굴복으로부터. 주기적
주기적인 시스템으로 인해 전체를 찾을 수있었습니다.
서로 가까이 있고 유용한 화학 원소 그룹
많은 질병(비소, 수은, 안티몬) 치료에 사용됩니다.
이러한 요소들은 19세기 말에 과학자들에게 다음과 같이 나타났습니다.
금광이 될 것이다. 동시에 과학자들은 완전히 사용했습니다.
Zinin의 화학 합성 원리와 Butlerov의 조합
원자와 분자의 배열에서.
합성 생산에 종사하는 의학자들 중
마약, 가장 큰 성공은 Ehrlich에게 돌아갔습니다.
Ehrlich는 평생을 지속적인 구현에 바쳤습니다.
하나의 아이디어 - 화합물로 얻은 것
몸에 해를 끼치 지 않고.
이 아이디어가 1891년에 표현되었다는 점을 강조하는 것이 중요합니다.
화학 요법의 창시자 D. L. Romanovsky. 그는 썼다,
그가 이상적인 약이라고 생각하는 것 ``
병든 신체에 주사하면 해가 가장 적습니다.
후자는 가장 큰 파괴적인 변화를 일으킬 것입니다.
손상 대리인 》. Romanovsky는 Earley의 아이디어를 예상했습니다.
하, 적을 쉽게 공격하는 '마법탄'에 대해요. 로마노프스키
정확한 관찰을 바탕으로 최초로 확립한
화학 요법의 가장 중요한 법칙은 직접적인 작용 메커니즘입니다
질병의 원인 물질에 대한 화학 약품.
`` 퀴닌, 말라리아 환자의 몸에 충분히 주입되면
쉽게 관찰할 수 있는 파괴적인 변화, 주로
이미지 - 핵심, 이 치료법이 사실로 간주되어야 하는 이유
말라리아에 대한 특정 의약품 》.
말라리아에 대한 이 치료법의 특이성은 질병의 본질에 대한 작용의 진정한 특이성을 반영합니다.
Romanovsky는 ``급진적 행동에 대한 질문을 처음으로 제기했습니다.
≫ 병원체에 대한 화학요법 약물 또는 그의 표현대로
〈 생산자〉 질병. 그러니까 그 사람이 창시자였지
훌륭한 살균 요법에 대한 아이디어.
퀴닌이 자연에 존재한다면 다음과 같이 추론한다.
인체의 경우 다른 것이 있어야합니다
다른 질병을 물리치는 데 사용할 수 있는 유사한 물질.
19세기 말에도 화학은 계속해서 발전해 나갔다.
로모노소프가 시작한 개선 행렬이 완료되었습니다.
지닌, 버틀레로프, 멘델레예프.
잡지는 새롭고 흥미로운 내용으로 가득 차 있었습니다.
화학의 정복에 대한 보고.
그러나 어디서부터 시작해야 할까요? 이미 획득한 수백개의 물질 중 어떤 물질이
화학적으로 합성에 사용될 수 있음
화학 요법?
아직 학생이었을 때 Ehrlich는 잘 알려진 실험을 반복했습니다.
이를 증명한 키예프 교수 가이벨(Geibel)
납중독의 경우, 이 금속은 고르지 않게 분포됩니다.
신체 내: 일부 기관에서는 눈에 띄게 납이 축적됩니다.
그러나 아무리 미세한 물질이라도 시체에서는 감지할 수 없습니다.
시약. 화학물질이 있다는 뜻이다.
선택적 행동이라고 Ehrlich는 결정했습니다.
그러나 Ehrlich는 납 실험을 포기했습니다.
눈으로 보기에는 중독된 세포도 건강한 세포와 다르지 않았습니다.
그는 메틸렌 블루 페인트를 선택했습니다.
관찰이 더 편리해질 것이며 말라리아 치료를 제안했습니다.
메틸렌 블루. 이 치료는 몇 가지 결과를 가져왔습니다.
Ehrlich는 그들에게 격려를 받고 실험을 확장하기 시작했습니다.
꼬리가 있고 말을 연상시키는 좁은 잎
쥐를 잡아 치명적인 질병을 일으켰습니다.
Erlich는 실험실에 앉아서 페인트의 상태를 확인하기 시작했습니다.
감염된 쥐. 이것은 아마도 단순화된 방법이었을 것입니다.
그러나 이것은 과학적 화학 요법의 첫 번째 단계였습니다. 어려운
동물 조건에 어떤 종류의 페인트가 있는지 즉시 확인하십시오.
한 페인트는 생쥐를 셔닐로 만들었고, 다른 페인트는 노란색으로 만들었습니다.
꼬리가 달린 트리파노솜은 여전히 혈류에 떠 있습니다.
쥐를 잡아 죽였습니다. 페인트로는 아무것도 나오지 않았습니다.
자연과학에서 '진리의 황금알'이 탄생하다
`` 수천 톤의 가공된 광석 ``에서. 열어보기만 하면 돼
어떤 치료법이든, 그러면 화학자는 그것을 분해하고 추가할 것입니다.
산 또는 알칼리, 시약과 연결, 원자 결정
체중은 아픈 동물에게 테스트할 것이고, 그 다음에는 사람에게도 테스트할 것입니다...
그리고 치료용 화학요법 약물 표에 나타납니다.
생명을 구하는 새로운 치료법.
합리적인 항암치료를 받기가 어려웠습니다.
올바른 방향으로 연결되는 나침반을 찾아야 했습니다.
길. 패턴을 찾아야 했어요...
그러던 어느 날, Erlich는 사무실에 앉아 책을 읽었습니다.
새로운 특허에 관한 화학 저널 최신호
수단. 독성이 없다는 뜻의 '아톡실(atoxyl)'이라고 불렸습니다.
이 약에 대한 실험은 다음과 같은 질병에 감염된 쥐를 대상으로 시작되었습니다.
트리파노솜.
수백 번의 실험 끝에 아톡실이
실제로 쥐를 치료합니다.
그러나 일부 쥐는 여전히 죽었습니다. 그러므로 그렇지 않다
따라서 아톡실은 이미 무해합니다.
Ehrlich는 그것을 무해하게 만들기로 결정했습니다. 이 제품은 가치가 있었습니다
그 일을 하기 위해서요.
아톡실(Atoxyl)은 벤젠 고리와 동일한 벤젠 고리를 포함하고 있습니다.
그리고 일부 색상.
벤젠 고리는 여섯 개의 탄소 원자가 서로 연결되어 있습니다.
한 원 안에. 그러나 산화비소가 첨가되었습니다.
이것은 분명히 약물 치료를 만들었습니다. 비소 - 알려진
독이지만 벤젠 고리와 결합하면
그것은 화학 요법 약물로 밝혀졌습니다.
그러나 이 독을 더 "고귀하게" 만드는 것이 필요했습니다.
더욱 안전하면서도 강력하게
병원체에 대한 치료법.
아톡실, 아톡실을 바꾸는 것은 불가능하다고 하더군요, 바로 거기에 있어요
무너질 것이다. 그러나 Ehrlich는 이 약을 변형시켰습니다.
수백 가지의 비소 제제를 방해하지 않고
벤젠과 비소의 조합.
그는 자신의 연구실에서 2년 동안 일했다.
혈액을 완전히 정화하는 치료법을 발견했습니다
그들을 죽인 사나운 트리파노솜에서 나온 쥐들. 동시에 새로운
이 제품은 쥐에게 무해한 것으로 밝혀졌습니다. 그 분들은 잘 참아주셨어요
〈 606〉 또는 살바르산, 그게 신약의 이름이었는데,
왜냐하면 그는 아톡실의 606번째 변종이었기 때문입니다. 이 약은
최고의 화학합성산물과 그 제조방법
폭발 및 화재의 위험이 있었습니다.
반응에 참여하는 수많은 화합물
미묘한 증기.
그리고 가장 중요한 것은 약물이 필요하다는 것을 입증하는 것이 가능했다는 것입니다
에어리스 앰플에 보관 - 공기가 혼합되어
유독하다.
이것은 화학적 이름이 dioc-인 약이었습니다.
Si-디아미노-아르세노벤젠-디하이드로클로라이드.
그런데 한 가지 중요한 사건이 일어났습니다.
Ehrlich의 연구 직전에 유명한 과학자 Shaw가 있습니다.
딘은 매독의 원인균인 스피로헤타 팔리듐(spirochete pallidum)을 발견했습니다.
트리파노소마 계열에서.
하지만 Erlich는 말에서 멈출 수 없다고 생각했습니다.
트리파노솜의 경우 스피로헤타에 영향을 미치는 것이 필요합니다.
사람에게 영향을 미치는.
그러나 그는 즉시 사람으로 전환하지 않았습니다. 그는 매독에 감염됐다
토끼를 잡아서 〈606〉이라는 약으로 치료했습니다. 후에
여러 번 주입하면 토끼는 아무것도 남지 않았습니다.
스피로헤타. 약물의 용량은 토끼에서도 개발되었습니다.
Ehrlich는 308개의 화합물을 더 생산하고 더 완벽한 화합물을 얻었습니다.
약물 - 〈 914 〉(네오살바르산). 이 약
5 입방 센티미터의 물에 용해되었습니다. 그의 소개
몸에 들어가는 것이 더 안전하다는 것이 밝혀졌습니다. 반응이있었습니다
약물은 여전히 일부 독성 특성을 유지했습니다.
일부 환자에서는 특히 고용량을 투여할 때
약물 〈 606〉 및 〈 914〉는 뇌 염증,
의식, 발열, 피부 출혈.
Ehrlich의 적들은 신약에 대해 소란을 피웠습니다.
그들은 Erlich에게 많은 문제를 일으켰습니다.
Ehrlich의 약물이 대규모로 테스트되었을 때
환자들에게 독성 효과가 있는 것으로 밝혀졌습니다
극히 드물다.
전 세계가 새로운 도구의 엄청난 중요성을 인식하고 있습니다.
매독은 더 이상 끔찍한 질병이 아닙니다. 치료가 준
훌륭한 결과; 환자의 궤양은 이후 사라졌다.
여러 주입.
에를리히는 재귀열의 스피로헤타제를 없애기로 결정했습니다.
매독 스피로헤타와 관련이 있다.
현재 러시아의 일부 도시에서는 다음과 같은 현상이 관찰되었습니다.
재열의 발생. 러시아 의사 Yu.
사라토프의 상트페테르부르크와 P.K. Galler는 대담한 결정을 내렸습니다.
세계 최초로 새로운 제품에 대한 폭넓은 테스트를 진행했습니다.
재발열 환자를 위한 약.
치료 효과는 놀라웠습니다. 환자가 치료된 후
40°의 온도에서 Ehrlich's 0.5g을 부었습니다.
약물을 투여한 후 14~6시간 후에 가장 강한 땀이 나기 시작했고
기온이 완전히 떨어졌습니다. 환자는 완전히 회복되었습니다.
그의 몸에는 스피로헤타가 완전히 없어졌습니다.
이것이 바로 과학자들의 대박멸균의 꿈이 실현된 것이 아닐까?
러시아 과학자들은 수년간 살바르산을 사용한 끝에
살바르산 주입 후
경미한 반응만 나타나지만 치명적인 합병증이 발생함
극히 드물다(100,000회 주입당 1명의 사망).
약물의 품질을 개선하고 올바른 설정을 확립합니다.
복용량과 정확한 금기 사항, 1916-917년에 작성됨
몇 년 동안 우리 과학자 G.I. Meshchersky, S.L.
새로운 - 이 치료법이 완전히 이루어질 것이라는 사실로 이어질 것입니다
안전한.
러시아의 고급 화학자 연구원과 의사들이 곧
에를리히의 발견 이후 그들은 스스로를 만드는 임무에 착수했습니다.
국내 살바르산.
V. K. Ferein 제약 실험실의 화학자 V. A. Smirnov
이미 1914년에 다음과 같은 유형의 우수한 무독성 약물이 탄생했습니다.
salvarsana. 유일한 단점은 약간 감소했습니다.
Ya. G. Shereshevsky, S. L. Bogrov가 생산한 쥐
S. S. Usoltsev et al., `` ben-
Zarsan 》은 환자 치료를 위해 진료소에서 사용되기 시작했습니다. 교수
T. P. Pavlov, G. I. Meshchersky 및 V. V. Ivanov가 출판한 여러 기사
1916-917년에는 "Russian Doctor", "Medical Newspaper" 및
``Russian Journal of Skin and Venereal Diseases''는 러시아 최초의 피부 및 성병에 대한 정보를 제공했습니다.
salvarsana 훌륭한 리뷰입니다.
이어 1916년부터 대량공장 생산이 조직화됐다.
러시아 살바르산 생산. 이번 제작은 유명 감독이 맡았다.
일반적으로 인정되는 원본을 개발한 러시아 화학자 P.F.
살바르산 합성 기술.
Smirnov와 동시에 러시아 Salvarsan('ar-라는 이름으로)
Ol»)은 1914년 모스크바 화학자 I. I. Ostromyslen-에 의해 합성되었습니다.
스키와 S.S. Kelbasinsky.
1915년에 "Russian Journal of Skin and Venereal Diseases"에서
이에 대해 Bogrov와 Meshchersky에 대해 매우 호의적 인 리뷰가있었습니다.
의약품.
사회주의 10월 대혁명 이후 설립되었다.
공장에서 러시아 salvarsan(novarsalan, novarsol) 생산
20세기에는 주기율표의 주요 하위족에 속한 원소가 보조 하위족에 위치한 원소보다 덜 인기가 있었습니다. 리튬, 붕소 및 게르마늄은 값비싼 이웃인 금, 팔라듐, 로듐 및 백금의 그늘에 있었습니다. 물론, 주요 하위 그룹 원소의 고전적인 화학적 특성은 전이 금속 착물이 참여하는 빠르고 우아한 과정과 비교할 수 없다는 점을 인정해야 합니다(이러한 반응의 발견으로 두 개 이상의 노벨상이 수여되었습니다). . 1970년대 초, 화학자들 사이에서는 주요 하위 그룹의 원소가 이미 모든 비밀을 밝혀냈으며 그들의 연구는 실제로 시간 낭비라는 의견이 일반적이었습니다.
숨겨진 화학혁명
이 기사의 저자가 학생이었을 때(그는 1992년에 카잔 대학교에서 졸업장을 받았습니다), 그와 그의 많은 친구들은 화학을 공부했습니다. 피-요소 부분이 가장 지루한 부분인 것 같았습니다. (이것을 기억하세요 에스-, 피- 그리고 디- 원자가 전자가 각각 점유되어 있는 원소 에스-, 피- 그리고 디-궤도.) 우리는 이러한 원소들이 지각에 어떤 형태로 존재하는지, 분리 방법, 물리적 특성, 전형적인 산화 상태, 화학적 특성 및 실제 적용에 대해 배웠습니다. 화학 올림피아드를 통과하고 학생으로서이 모든 유용한 정보를 배운 사람들에게는 두 배로 지루했습니다. 아마도 이것이 우리 시대에 전문 분야를 선택할 때 무기 화학과가 그다지 인기가 없었던 이유일 것입니다. 우리 모두는 유기물 또는 유기 원소 전문가에게 들어가려고 노력했으며, 그곳에서 그들은 화학에 등장한 전이 금속 시대에 대해 이야기하고 상상할 수 있는 모든 것을 촉진했습니다. 그리고 상상할 수 없는 물질의 변형.
그 당시에는 컴퓨터도 인터넷도 없었습니다. 우리는 우리 도서관이 구독하는 화학 초록 저널과 일부 외국 저널에서만 모든 정보를 받았습니다. 우리나 우리 선생님들은 1980년대 말에 주요 하위 그룹 원소의 화학 르네상스의 첫 징후가 이미 눈에 띄게 되었다는 사실을 알지 못했습니다. 그때 그들은 이국적인 형태를 얻는 것이 가능하다는 것을 발견했습니다. 피-원소 - 저배위 및 저산화 상태의 실리콘 및 인이지만 동시에 실온에서 매우 안정적인 화합물을 형성할 수 있습니다. 그 당시에는 실제 사용이 논의되지 않았지만 이러한 물질 합성의 첫 번째 성공적인 예는 주요 하위 그룹 요소의 화학이 약간 과소 평가되었으며 아마도 다음과 같은 때가 올 것이라는 것을 보여주었습니다. 피-그림자에서 요소가 나타날 수 있습니다. 디-그리고 심지어 에프-강요. 결국, 그런 일이 일어났습니다.
1981년은 주요 하위 그룹 요소로의 전환의 시작점으로 간주될 수 있습니다. 그 당시, 이 화학 결합의 파트너 중 하나(또는 둘 다)가 두 번째 기간의 요소인 경우에만 안정적인 이중 또는 삼중 결합이 형성될 수 있다는 생각을 반박하는 세 편의 작품이 출판되었습니다. 이 "이중 결합의 법칙"은 위스콘신 대학의 로버트 웨스트(Robert West)에 의해 처음으로 반박되었습니다. 그 그룹에서는 모든 사람에게 친숙한 알켄의 더 무거운 유사체인 실리콘-실리콘 이중 결합을 가진 화합물인 안정적인 실렌을 최초로 합성했습니다. 유기화학에서 ( 과학, 1981, 214, 4527, 1343–1344, 도이: 10.1126/science.214.4527.1343). 그 후 얼마 지나지 않아 요시후지 마사아키(Masaaki Yoshifuji)가 이끄는 도쿄 대학의 연구자들은 인-인 이중 결합을 갖는 화합물의 합성을 보고했습니다. , 1981, 103, 15, 4587~4589; doi:10.1021/ja00405a054). 같은 해 슈투트가르트 대학의 게르트 베커(Gerd Becker)는 인-탄소 삼중 결합을 갖는 화합물인 안정한 포스팔알킨을 얻을 수 있었는데, 이는 카르복실산 니트릴의 인 함유 유사체로 간주될 수 있습니다. Zeitschrift für Naturforschung B, 1981, 36, 16).

인과 규소는 세 번째 기간의 원소이므로 아무도 그러한 능력을 기대하지 않았습니다. 후자의 화합물에서 인 원자는 배위적으로 불포화되어 있기 때문에 우리는 인 원자나 그 유사체가 촉매로 사용될 수 있기를 바랐습니다. 희망의 이유는 촉매의 주요 임무가 활성화되어야 하는 기질 분자와 접촉하는 것이며, 시약이 쉽게 접근할 수 있는 분자만이 이를 수행할 수 있고 대부분의 화학자에게 친숙한 인산염인 인 원자에 있다는 것입니다. 4개의 그룹으로 둘러싸인 는 결코 접근 가능한 센터라고 할 수 없습니다.
가장 중요한 것은 체적 환경입니다.
1981년에 발표된 세 가지 합성은 모두 새롭고 이국적인 화합물에서 주요 하위족 원소를 둘러싼 치환기가 올바르게 선택되었기 때문에 성공했습니다(전이 금속 화학에서는 치환기를 리간드라고 함). West, Yoshifuji 및 Becker가 얻은 새로운 파생물에는 한 가지 공통점이 있었습니다. 즉, 주요 하위 그룹의 원소와 관련된 부피가 큰 리간드가 다른 상황에서는 안정되지 않는 낮은 배위 상태의 실리콘 또는 인을 안정화했다는 것입니다. 벌크 치환기는 공기 중의 산소와 물로부터 실리콘과 인을 보호하고, 또한 불균형 반응에 들어가고 일반적인 산화 상태(실리콘과 인의 경우 각각 +4 및 +5)와 배위수(실리콘과 인의 경우 4)를 취하는 것을 방지합니다. 두 요소 모두). 따라서 실렌은 4개의 부피가 큰 메시틸 그룹(메시티는 1,3,5-트리메틸벤젠임)에 의해 안정화되고, 포스파알킨은 부피가 큰 tert-부틸 치환기에 의해 안정화되었습니다.
부피가 큰 리간드가 화합물을 안정화시키는 것이 분명해지면 피-원소가 낮은 산화도 및/또는 낮은 배위수를 갖는 경우, 다른 과학자들이 주요 하위 그룹 원소의 새롭고 특이한 파생물을 얻는 데 참여하기 시작했습니다. 2000년대 이후 거의 모든 이슈에서 과학(그리고 2009년 잡지가 나온 이후로 자연화학- 거의 모든 문제에서) 주요 하위 그룹의 요소와의 이국적인 조합이 보고됩니다.

따라서 최근까지 누구도 안정적인 실릴렌(규소 함유 카르벤 등가물)을 얻고 특성화하는 것이 가능할 것이라고 생각하지 못했습니다.
카르벤은 2가 및 이중 배위 탄소 원자가 전자 쌍(보다 안정적인 단일항 카르벤) 또는 두 개의 분리된 짝을 이루지 않은 전자(보다 반응성이 높은 삼중항 카르벤)를 갖는 반응성이 높은 종입니다. 2012년에 호주 Monash 대학의 Cameron Jones와 옥스포드 및 University College London의 동료들은 부피가 큰 붕소 리간드에 의해 안정화되는 최초의 단일항 실릴렌 - 2가 실리콘을 기술했습니다. 미국 화학 학회지, 2012, 134, 15, 6500–6503, doi: 10.1021/ja301042u ). 실릴렌은 결정 상태로 분리될 수 있으며 최대 130°C의 온도에서도 안정적으로 유지된다는 점은 주목할 만합니다. 그러나 용액에서는 카르벤 이량체의 실리콘 유사체가 실렌을 형성하거나 알칸의 C-H 결합에 도입되어 카르벤 유사체의 화학적 특성을 재현합니다.
화학자들은 주요 하위 그룹의 원소를 포함하는 새로운 유기 화합물을 계속해서 얻고 있습니다. 특히, 그들은 잘 알려진 구조에서 두 번째 기간의 요소를 이전 기간의 유사한 요소로 대체하려고 시도하고 있습니다. 물질). 또 다른 방향은 희귀 우표를 수집하는 것과 약간 비슷합니다. 우표 대신 화학 구조가 있습니다. 예를 들어, 2016년에 옥스포드의 Alexander Hinz는 4개의 서로 다른 닉토젠(질소에서 비스무트까지 주요 하위 그룹의 5번째 그룹 요소)의 원자를 포함하는 순환을 얻으려고 했습니다. 그는 문제를 완전히 해결하지 못했습니다. 선형 구조를 가진 분자는 순환에 닫히지 않았습니다. 하지만 5개 중 4개를 포함해 독특한 Sb-N-As=P 사슬을 지닌 분자도 인상적이다. 피-질소 하위 그룹의 요소 ( 화학. 유럽 저널, 2016, 22, 35, 12266–12269, doi: 10.1002/chem.201601916 ).

물론, 주요 하위 그룹 요소의 이국적인 파생물 합성을 "화학적 수집"으로만 이야기하는 것은 불가능합니다. 왜냐하면 오래된 시대의 요소를 포함하는 잘 알려진 유기 화합물의 유사체를 얻는 것이 구조 이론을 명확히하는 데 확실히 중요하기 때문입니다. 화학 결합의. 물론 이것이 화학자들의 관심의 유일한 이유는 아닙니다. 이러한 물질이 실제로 사용될 수 있는 영역을 찾으려는 욕구는 바로 주요 하위 그룹 원소의 화학 르네상스의 이유입니다.
1980년대에 낮은 배위가 관찰된 최초의 물질 합성 이후 피-화학자들은 그러한 배위 불포화 화합물이 전이 금속 착물과 같은 방식으로 많은 반응을 촉매할 수 있기를 바랐습니다. 고가의 백금 및 팔라듐 화합물을 주요 하위 그룹의 원소만 포함하는 분자로 교환하는 것은 매우 유혹적일 것입니다. 금세기에 이미 나타난 특이한 화합물의 특성에 대한 정보 피-요소는 이론적 예측을 확인했습니다. 그들 중 다수는 탄화수소, 분자 수소 및 이산화탄소를 활성화시키는 것으로 나타났습니다.
전이금속이 왜 나쁜가요?
전이 금속 유도체에 의해 오랫동안 완벽하게 가속화된 공정을 위한 새로운 촉매를 개발하는 이유는 무엇일까요? 또한, 전이 원소의 유기금속 화학은 가만히 있지 않습니다. 반응성의 새로운 측면이 항상 발견되고 있습니다. 디-강요. 그러나 귀금속 전이금속에는 단점도 있습니다. 우선, 가격입니다. 유기 및 유기 원소 화합물의 변환에 가장 효과적인 촉매는 로듐, 백금 및 팔라듐의 복합체입니다. 두 번째 어려움은 백금과 팔라듐의 천연 매장량이 고갈된다는 것입니다. 마지막으로, 백금이나 팔라듐 촉매의 또 다른 문제는 높은 독성입니다. 미량의 전이 금속에서도 물질을 정제하는 데 드는 비용으로 인해 가격이 크게 상승하기 때문에 약물을 얻을 때 특히 그렇습니다. 새로운 촉매로의 전환은 최소한 약물 물질의 비용을 크게 줄이고 목표 반응 생성물의 정제를 단순화할 수 있습니다.
주요 하위 그룹의 원소를 기반으로 한 촉매를 사용하면 추가적인 이점이 제공될 수 있습니다. 따라서 일부 알려진 반응이 더 온화한 조건에서 일어날 가능성이 있으며 이는 에너지를 절약하는 것이 가능하다는 것을 의미합니다. 예를 들어, 1981년에 최초의 실렌의 합성과 특성에 관한 연구에서 Jones는 실리콘-실리콘 이중 결합을 가진 화합물이 실온보다 훨씬 낮은 온도에서도 수소를 활성화할 수 있다는 사실을 입증했습니다. 고온 사용.
새천년에 발견된 중요한 화학 공정 중 하나는 게르마늄을 함유한 알킨 유사체인 디게르민(digermin)의 도움으로 분자 수소를 활성화하는 것입니다. 미국 화학 학회지, 2005, 127, 12232–12233, doi: 10.1021/ja053247a). 평범해 보일 수 있는 이 과정은 두 가지 이유로 흥미롭다. 첫째, 알킨과 발아의 구조가 유사함에도 불구하고 수소는 탄소-탄소 삼중 결합을 갖는 탄화수소의 시나리오 특성에 따르지 않고 후자와 반응합니다(수소는 삼중 결합의 각 원자에 부착되고 발아는 게르멘), 그러나 전이 금속 원자에 대한 전형적인 메커니즘을 따릅니다. 수소 분자가 원소에 부착되고 두 개의 새로운 E-H 결합(설명된 경우 Ge-H)이 형성되는 이 메커니즘을 산화 첨가라고 하며 전이 금속과 관련된 많은 촉매 공정의 핵심 단계입니다. 둘째, H2는 가장 단순하고 복잡하지 않은 분자처럼 보일 수 있지만 H2의 화학 결합은 두 개의 동일한 원소 사이에서 발생할 수 있는 모든 것 중에서 가장 강력하므로 이 결합이 끊어지고 이에 따라 촉매 수소화 공정에서 수소가 활성화됩니다. 화학기술의 관점에서 보면 결코 간단한 일이 아니다.
수락자를 기증자로 만드는 것이 가능합니까?
원소가 수소의 산화적 첨가를 겪으려면(주기율표의 위치에 관계없이) 전자 구조의 특정 특징을 가져야 합니다. E + H 2 = H-E-H 과정은 원소가 배위 불포화이고 자유 궤도가 분자 수소의 전자를 수용할 수 있는 경우에만 발생합니다. 더욱이, 이 자유 궤도의 에너지는 전자를 포함하는 수소의 분자 궤도의 에너지에 가까워야 합니다. 균질 금속 착물 촉매 분야의 발전은 화학자가 금속과 관련된 리간드의 구조를 변경하여 궤도의 에너지를 변화시켜 반응에 참여하는 엄격하게 정의된 물질에 맞게 "조정"할 수 있다는 사실로 주로 설명됩니다. . 오랫동안 궤도 에너지의 부드러운 조정은 다음과 같은 경우에만 가능하다고 믿어졌습니다. 디-그러나 지난 10년 동안 요소들에 대한 것으로 밝혀졌습니다. 피- 요소도요. 연구자들은 발톱과 같은 리간드가 배위 중심을 잡는 질소 함유 복합체에 가장 큰 기대를 걸고 있습니다(라틴어 c에서 킬레이트 리간드라고 함). 헬라,발톱) 및 상대적으로 새로운 종류의 리간드를 사용합니다. N-헤테로고리형 카르벤.

후자의 성공적인 예는 캘리포니아 대학교 샌디에고 캠퍼스의 Guy Bertrand의 연구인데, 이 연구에서는 이러한 리간드가 붕소 원자를 안정화시켰습니다. 과학, 2011, 33, 6042, 610–613, doi: 10.1126/science.1207573). 일반적으로 외부층에 3개의 전자만 포함하는 붕소 유도체는 고전적인 전자 수용체(루이스산) 역할을 합니다. 사실 붕소는 안정적인 8개의 전자 껍질에 도달하려면 5개의 전자가 더 필요하므로 자신의 전자 3개와 제3의 전자 3개로 3개의 공유 결합을 형성할 수 있지만 다른 사람의 전자를 받아들임으로써 2개의 전자를 더 얻어야 합니다. 빈 전자 세포와 쌍을 이룹니다. 하지만 N-헤테로고리형 카르벤은 매우 강력한 전자 공여체이므로 그와 결합된 붕소는 더 이상 수용체 역할을 하지 않습니다. 이는 너무 "전자가 풍부한" 상태가 되어 루이스 산에서 루이스 염기로 변합니다. 최근까지 화학자들은 잘 알려진 물질의 특성이 이렇게 크게 변할 것이라고 예측조차 할 수 없었습니다. 피-요소. 그리고 Bertrand의 작업은 이론적 관점에서만 여전히 흥미롭지만, 우리 시대의 이론에서 실천으로의 전환은 매우 빠르게 일어나고 있습니다.
촉매작용까지는 얼마나 됩니까?
따라서 최근에 합성된 주요 하위 그룹 원소의 파생물은 전이 금속 착물을 촉매하는 주요 반응에 들어갈 수 있습니다. 불행하게도 앞서 언급한 규소 또는 붕소 원자에 분자 수소의 산화적 첨가조차도 완전한 촉매 순환을 위해 전개되어야 하는 일련의 반응 중 첫 번째 단계일 뿐입니다. 예를 들어, 주요 하위 그룹의 화합물이 존재할 때 수소화에 관해 이야기하는 경우, 그 메커니즘은 윌킨슨 촉매가 있을 때 수소 첨가 메커니즘을 재현한 다음 수소와의 상호 작용 후에 피-원소는 알켄과 착물을 형성해야 하며, 수소화물 이동과 착물화가 일어나야 하며, 궁극적으로 최종 생성물의 형성과 촉매 활성 종의 재생으로 이어질 다른 모든 단계가 발생해야 합니다. 그래야만 하나의 촉매 입자가 수십, 수백 또는 수천 개의 목표 생성물 분자를 생성합니다. 그러나 이러한 촉매 사이클이 작동하려면 더 많은 문제를 해결해야 합니다. 산화 첨가의 결과로 형성된 원소-수소 결합은 너무 강하지 않아야 합니다(그렇지 않으면 수소화물 이동이 발생하지 않음). 수소는 알켄 등과의 상호작용을 위해 저배위 상태를 유지해야 합니다. 한 순간이라도 놓치면 촉매제는 사라진다 피- 요소의 동작이 유사함에도 불구하고 요소가 작동하지 않습니다. 디-일부 프로세스의 요소.
금속 착체 촉매 작용에서 주요 하위 그룹 원소의 화합물에 의한 촉매 작용으로의 전환은 너무 어려운 작업이며 완료되기까지 매우 먼 것처럼 보일 수 있습니다. 그러나 화학에 대한 관심 피- 백금이나 팔라듐 촉매를 다른 것으로 대체하려는 합성 화학자들의 욕구와 원소는 확실히 이 방향에 돌파구를 제공할 것입니다. 향후 10년 내에 주요 하위 그룹의 배위 불포화 원소를 기반으로 하는 촉매에 대해 듣게 될 가능성이 있습니다.
2011년 초 IUPAC는 LLNL(미국)과의 JINR 협력이 114번 및 116번 원소 발견에 우선순위가 있음을 인정했습니다. 원소 114 - Flerovium, Fl; 116요소 ― 리버모리움, Lv.
Flerovium - 핵반응연구소의 이름을 딴 것입니다. 초중원소 합성 분야의 선두주자인 G.N. Flerov JINR과 창립자이자 뛰어난 물리학자 G.N. Flerov(1913-1990) - 중금속의 자연분열에 대한 새로운 유형의 방사능 발견의 저자 수많은 새로운 과학적 방향의 창시자이자 현재 그의 이름을 딴 FLNR JINR의 창시자이자 첫 번째 이사인 Nuclei.
리버모리움(Livermorium) - 리버모어 국립 연구소를 기리기 위한 것입니다. 로렌스와 그 위치 - 리버모어시 (미국 캘리포니아). 리버모어 과학자들은 20년 넘게 Dubna에서 진행된 새로운 원소 합성 실험에 참여해 왔습니다.
일반적으로 IUPAC 결정은 현대 핵물리학의 가장 중요한 성과 중 하나인 초중원소의 "안정도 섬" 발견에 대한 JINR 과학자들의 뛰어난 공헌을 인정한 것입니다.